発表のポイント
- 細胞がくっつきやすく逃げ出しにくい極小の「水たまり」を、生体材料(ポリジメチルシロキサン)に電子線を照射するだけで簡単に作製することに成功した。
- 「水たまり」は細胞を1細胞レベルで任意の場所・形状に捕捉することができるため、迅速かつ低コストな診断や創薬に役立つことが期待される。
国立研究開発法人量子科学技術研究開発機構(理事長 平野俊夫、以下「量研」という。)量子ビーム科学研究部門高崎量子応用研究所先端機能材料研究部の大山智子主任研究員・田口光正プロジェクトリーダーらは、生体材料1)のポリジメチルシロキサン(PDMS)2)に電子線を照射して、わずかピコリットル(1兆分の1リットル)レベルの「水たまり」が作れる長期間安定な親水性表面を持つ凹構造を作製し、細胞1個を任意の場所・形状に簡単につかまえる技術を開発しました。先端医療分野で需要が高まる「細胞を1つ1つ分離して捕捉するデバイス」を実現する本技術により、少量の検体・試薬で細胞分析や薬剤スクリーニングを行ったり、任意の場所・形状に細胞を集めて安定に長期培養したりといったことが可能になり、迅速かつ低コストな診断や創薬、再生医療といった様々な分野への応用展開が期待されます。
PDMSはバイオデバイス3)基材として有力な材料ですが、水や細胞をはじく欠点(疎水性)を有しています。また、表面を親水化処理しても、その効果が急激に失われることが大きな問題でした。それを改善するために、本研究では55kVの低エネルギー電子線4)を大気中で照射してPDMS表面に分解・架橋・酸化反応を引き起こし、細胞接着に適した酸化ケイ素に似た構造の親水化層を厚さ40µmの領域に形成することに成功しました。この親水化層では、培養環境下で1ヵ月以上も処理効果を維持することができます。さらに、親水化層は未照射のPDMSに比べ収縮することから、化学薬品を一切使わずに、数分の照射だけで局所的に親水化した深さ数10µmの凹構造を簡単に作製することができるようになりました。
照射された凹部以外は疎水性であり、液体は凹部に優先的に入って内部に留まるため、水をかけるだけで自動的に小さな「水たまり」ができます。そのため、細胞を簡単に周りの液体(培地)ごと「水たまり」の中に捕捉することができるのです。また、「水たまり」の内部は細胞接着に適した表面を有しているため、細胞を1つ1つ「水たまり」の内部だけに接着させることが可能になりました。一細胞レベルで簡便に細胞を捕捉して安定に長期培養できる本技術は、診断・創薬・再生医療など様々な先端医療分野への応用展開が期待されます。
本成果は、応用物理学の専門誌「Applied Physics Letters」に2018年5月28日(予定)にオンライン掲載されます。
本研究の背景と目的
先端医療やバイオ研究に不可欠なバイオデバイスの開発では、細胞接着性をはじめとする特定の機能を自由に制御できる生体材料の創製がカギとなります。しかし生体材料は熱や化学処理に弱いものが多く、生体親和性を失わずに性質を変えたり、精密に加工したりすることは困難でした。そこで量研では、各種量子ビームを駆使することでこの問題を解決し、機能化と微細加工という2つの技術の融合による先端材料の開発を進めてきました。
我々は今回、生体材料の一種であるPDMSを量子ビームで親水化・微細加工することにより、診断・創薬分野で需要が高まる「細胞を1つ1つ分離して捕捉するデバイス」の実現に向け、長期にわたって安定な親水性表面を持つ凹構造を作製して、細胞を任意の場所・形状に簡単につかまえる技術を開発しました。PDMSは透明で自家蛍光5)が低く、安価なため、バイオデバイス基材として有力な材料ですが、水や細胞をはじく(疎水性)という大きな欠点があります。そこで材料表面に効率よくエネルギーを付与することができる低エネルギー電子線によって、PDMSを細胞培養に適した表面状態に変化させるだけでなく、細胞がくっつきやすく逃げ出しにくいように加工して、細胞をつかまえることができないか検討しました。
研究手法と成果
1.「水たまり」の作製と特徴
厚さ1mmのPDMSフィルムに対し、55kVの電子線を330kGy/sで大気中照射したところ、照射量に応じて水の接触角6)が低下し、表面が疎水性から親水性に変化することが分かりました(図1a)。例えば30秒間照射すると、接触角は110°から65°に変化し、線維芽細胞の接着に適しているとされる接触角60~70°の範囲に改善することができます。
この電子線照射による親水化には、2つの大きな特徴があることが分かりました。
1つ目の特徴は、親水化表面を長期にわたって維持できるという点です。PDMSはガラス転移温度7)が低い柔らかいゴム材料で、室温では分子が動き回るために表面状態は刻一刻と変化します。例えば、一般的な親水化処理法であるプラズマ照射をPDMSに適用すると、照射直後から急激に親水性が失われることが知られています(図1b)。そのため、使用直前の処理が必要であるだけでなく、処理効果の再現性も低いことが大きな問題でした。一方、電子線による親水化処理は非常に安定で、細胞培養環境下で1ヵ月以上も親水性が持続することが確認されました(図1b)。
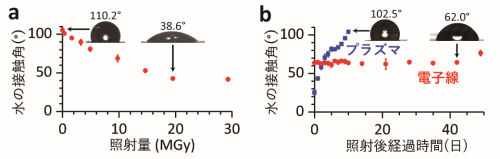
図1.電子線照射によってPDMSを親水化し、その度合いを制御することができました(a)。さらに、親水化の効果は非常に安定で、細胞培養環境下で1ヵ月以上も親水性が持続することが確認されました(b)。
2つ目の特徴は、照射されて親水化した部分が数十µm凹むということです。この特徴を利用すれば、マスクを使って電子線を照射するだけで、疎水性のPDMSフィルム上に、親水性を持つ凹パターンを形成することができます。液体は深さ数十µmの凹部に優先的に入り、中に留まります。そのため、水をかけるだけで自動的に「水たまり」ができ、狙った箇所に水滴を並べることができるようになります(図2)。「水たまり」のサイズや形状はマスクによって変えることができ、また親水化の度合いは照射条件によって制御することができます。
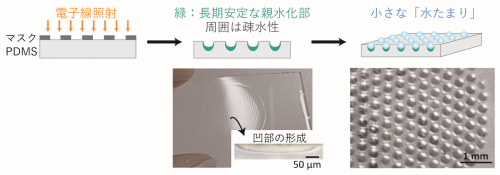
図2.マスクを使って電子線を照射するだけで、PDMSを微細加工すると同時に照射部分を親水化できます。照射されない部分は疎水性を保つため、親水性を持つ凹部に水が優先的に入り、中に留まることによって、水をかけるだけで自動的に「水たまり」ができます。
「水たまり」ができる理由、つまり、電子線照射によってPDMSが長期間安定な親水性を持つようになり、同時に凹構造が形成される理由は、電子線のエネルギー付与分布にありました。分析の結果、電子線照射によって、PDMS表面から約40µmの深さにかけて疎水性の原因であるメチル基(–CH3)が減少する一方、酸素が導入され、酸化ケイ素に似た構造の親水化層が形成されたことが分かりました。一般的な酸化処理であるプラズマで形成できる親水化層が100nm程度であることを踏まえると、400倍程度厚い層です。この厚い親水化層が、その下にある疎水性のPDMS分子が表層に出てくること(分子の再配列)を妨げるために、電子線を照射したPDMS表面は長期間安定な親水性を示すと考えられます。また、電子線を照射しただけで凹構造が形成される理由は、照射によって形成された親水化層が未照射のPDMSに比べ収縮するためです。親水化層の形成と収縮は照射中に同時に起こるため、数10µmの深さを持つ凹構造の底からさらに約40µmの深さにかけて親水化層が形成されます(図2)。
長期安定な親水性を持つ「水たまり」は、電子線がPDMS中に誘起する酸化・分解・架橋といった反応を最大限に活かし、制御することによって実現したのです。
2.「水たまり」に細胞をつかまえる
化学薬品を一切使わないためPDMSの生体適合性を損なうことなく、電子線照射の1工程だけで長期安定な親水性を持つ凹構造を作製するこの技術は、細胞を捕捉し、任意の場所・形状で培養するマイクロウェル8)として応用することができます。例えば、直径数十µmの凹構造を並べれば、市販の96ウェルマイクロプレート(直径7mm)のおよそ数万倍となる数100万マイクロウェル培養プレートをわずか数分で作製することが可能です。この時、凹構造に溜まる「水たまり」の液量はわずかピコリットルレベルで、使用する検体や試薬を大幅に削減することができます。
電子線を照射したPDMSフィルムに細胞をまき、細胞が沈むのを待って余分な培地を吸い取るだけで、細胞は簡単に「水たまり」の中に捕捉されます(図3a)。これは細胞が周りの液体(培地)ごと親水性を持つ凹構造の中に留まる現象を利用した捕捉法ですが、凹構造内外の細胞接着性の違いを利用することも可能です。細胞は適度な親水化面を持つ凹構造の内部に優先的に接着する一方、凹構造の外は疎水性のため細胞をはじきます。そのため一定時間培養後に接着していない細胞を洗い流すと、凹構造内部にのみ細胞が残るのです。この手法により、我々は1細胞レベルで細胞を捕捉することに成功しました(図3b)。任意の場所・形状に簡単に細胞を配置する技術の開発によって、少量の検体・試薬で迅速な細胞分析を行ったり、細胞を集めて細胞塊や組織を培養したりといった最先端の細胞培養が可能になります。
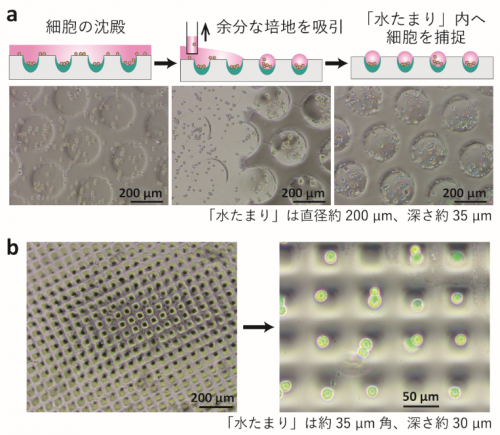
図3.細胞播種後、細胞が沈むのを待って余分な培地を吸い取るだけで、細胞は簡単に「水たまり」の内部に捕捉されます(a)。また、凹構造内外の細胞接着性の差を利用して、1細胞レベルで細胞を捕捉することにも成功しました(b)。
今後の展開
電子線がPDMS中に誘起する酸化・分解・架橋といった反応を最大限に活かし、制御することによって、PDMS表面に長期安定な親水化表面を持つ凹構造を作り出して細胞をつかまえる新技術を開発しました。ピコリットル~ナノリットルの液滴を溜められる微小な「水たまり」は、細胞1つ1つを捕捉し、任意の場所・形状で安定に培養することが可能です。生命の謎に迫る細胞生物学から、迅速な診断や創薬、再生医療といった幅広い分野への応用展開が期待されます。
なお、本成果はJSPS科研費若手研究(B) 26790070(代表:大山智子)の助成を受けて行い、2017年6月8日に岩崎電気株式会社と共同で特許を出願しました(特願2017-113092「試験用基材、及び試験用基材の製造方法」)。
用語解説
1)生体材料
医療器具等への利用が可能な、生体に害を及ぼさず、生体に親和性が高い材料を指します。
2)ポリジメチルシロキサン(PDMS)
シリコーンゴムの一種で、生体材料の一つです。胃腸の消泡剤として医薬品に使われるほか、透明で自家蛍光3)が低く、安価であることから、マイクロ流路や各種バイオデバイス用基材、パターン形成・転写時の型やスタンプとして、ナノ・マイクロデバイスの加工・製造に広く利用されています。
3)バイオデバイス
微細加工技術によって細胞やバイオ分子を制御したり、機能を解析したりするためのデバイスの総称です。
4)低エネルギー電子線
一般的に、300kV以下で加速された比較的低いエネルギーを持つ電子線を指します。
5)自家蛍光
光を吸収した際に自然に光を放出する性質を指します。自家蛍光が強いと顕微鏡観察を妨げるため、バイオデバイスの基材には自家蛍光が低い材料が望まれます。
6)水の接触角
水へのなじみ(濡れやすさ、親水性)の基準です。水を滴下し、水滴と材料が成す角度によって評価されます。水によくなじむ親水性の材料の場合、この角度は小さくなります。逆に、撥水性の材料では水滴の形状は球に近づくため、角度は大きくなります。一般的に、接触角が90°未満の材料を親水性、90°以上の材料を疎水性と呼びます。
7)ガラス転移温度
硬く流動性がない状態(ガラス)から、粘度が下がり軟化し始める境目の温度を指します。
8)マイクロウェル
細胞培養に用いる容器の中でも特に小さいものです。96マイクロウェルは、直径7mmの容器(くぼみ)が96か所配置されたプレートです。
論文について
Single-step fabrication of polydimethylsiloxane microwell arrays with long-lasting hydrophilic inner surfaces
執筆者・所属
Tomoko Gowa Oyama1, Bin Jeremiah Duenas Barba2, Yuji Hosaka1, and Mitsumasa Taguchi1
- 国立研究開発法人量子科学技術研究開発機構 量子ビーム科学研究部門
- Philippine Nuclear Research Institute, Department of Science and Technology
