発表のポイント
- 膵臓がん細胞に放射線を照射すると、細胞自身がもつ生存メカニズムの細胞周期チェックポイント1)の活性化と、それに依存したオートファジー2)の誘導が起こることを解明した
- 膵がんモデルマウスで、細胞周期チェックポイントの働きを薬剤で阻害して放射線治療をすると治療効果が向上することを明らかにした
- 放射線治療が効かず、予後が非常に悪い膵臓がんに対する放射線治療効果を増感する方法の開発に繋がることが期待される
国立研究開発法人量子科学技術研究開発機構(理事長 平野俊夫。以下「量研」という。)量子生命・医学部門量子医科学研究所 重粒子線治療研究部 放射線がん生物学研究グループの長谷川純崇グループリーダー・鈴木基史研究員(現、関西医科大学)・安康真由香協力研究員らは膵臓がん(膵がん)の放射線治療に対する抵抗性のメカニズムの一端を明らかにしました。
膵がんは近年増加傾向にあるがんです。早期の発見が難しく、放射線治療をはじめとする現在のがん治療に対して非常に抵抗性を示すがんです。そのため、5年生存率は10%以下で予後が非常に悪いことが特徴です。
量研では「がん死ゼロ健康長寿社会の実現」を目指して、働きながら治療出来、切らずに治す量子メス3)の研究開発を行っています。膵がんは最優先で克服すべき戦略がんとして位置づけており、その克服に向けて新たな早期診断や治療法を開発するため、膵がんの放射線治療に対する抵抗性メカニズムの解明を目的とした基礎研究を行っています。
膵がんの放射線抵抗性のメカニズムとして、細胞自身が有するオートファジーと細胞周期チェックポイントという細胞生存に関わる機能の関与が示唆されています。細胞周期チェックポイントの働きを阻害すると放射線抵抗性が弱まることはわかっていましたが、がん細胞におけるオートファジーの働きは複雑で良くわかっていませんでした。
そこで研究グループは、この細胞周期チェックポイントとオートファジーが協調して働くことにより膵がん細胞が放射線抵抗性を示すのではないか、との仮説を立て、両者の関係を調べました。その結果、放射線照射による細胞周期チェックポイント4)の活性化に依存してオートファジーが働くことを明らかにしました。更に、膵がんモデルマウスに細胞周期チェックポイントを阻害する薬剤を投与して放射線治療を行うことで、膵がんの放射線抵抗性が弱まり、治療効果が向上することも明らかにしました。本成果は、放射線治療が効きにくく、予後が非常に悪いがんの一つである膵臓がんに対する放射線治療効果を増感する方法の開発に繋がることが期待されます。
この成果は、放射線腫瘍学(放射線がん治療)の分野でインパクトの大きい論文が数多く発表されている「International Journal of Radiation Oncology, Biology, Physics」に2021年6月7日(月)21:00(日本時間)にオンライン掲載されました。
研究の背景と目的
膵がんは近年増加傾向にあるがんの一つです。早期発見が非常に難しく、また、がん細胞自体の悪性度も高いため、手術で完全切除すること以外、現状のがん治療法では完治が難しく、難治性がんの代表例となっています。5年生存率は10%にも満たず、予後も非常に悪くなっています。放射線治療にも抵抗性のがんであり、放射線抵抗性のメカニズムを解明することは、放射線治療の有効性を確立するためにも重要です。
研究グループは、放射線抵抗性を決定づける因子として、細胞周期チェックポイントとオートファジーに着目しました。細胞周期チェックポイントは細胞周期を進めてよいかどうかの細胞内監視機構であり、放射線により細胞が傷つくと細胞周期チェックポイントが活性化して放射線で傷ついたDNAを修復するために細胞周期を止めます。オートファジーは細胞内外からのストレスに応じて働く自食作用で、自己の細胞内小器官やミトコンドリアなどを分解して得られるATP(アデノシン三リン酸)5)を再利用して細胞の生存を維持します。両方とも細胞自身が保持している生物学的メカニズムであり、細胞内外からのストレスに対して防護的に働き、細胞生存に関与しています。
膵がん細胞の放射線抵抗性は、これらの細胞生存メカニズムがそれぞれ独立して働くことによるものと考えられており、細胞周期チェックポイントの働きを阻害すると放射線抵抗性が弱まることはわかっていましたが、がん細胞におけるオートファジーの働きは複雑で良くわかっていませんでした。研究グループは、この細胞周期チェックポイントとオートファジーが協調して働くことにより膵がん細胞が放射線抵抗性を示すのではないか、との仮説を立てました(図1)。
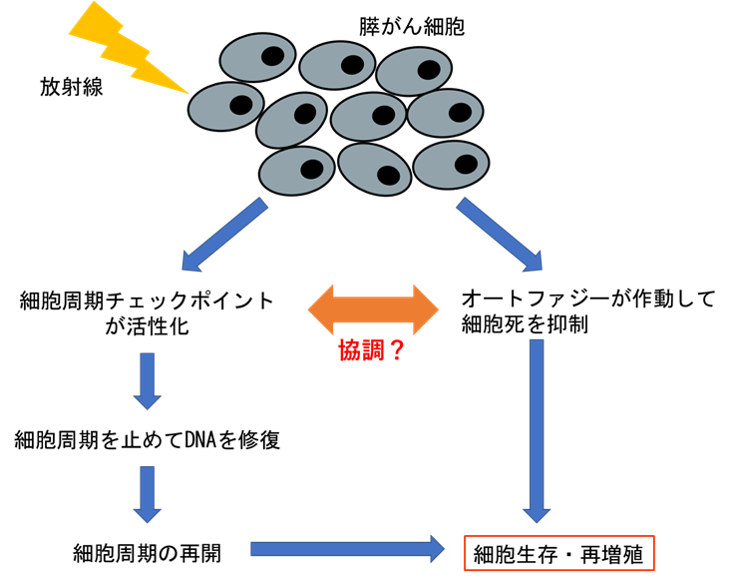
図1 膵がんの放射線抵抗性メカニズムに関する仮説
そこで、放射線照射された膵がん細胞での細胞周期チェックポイントとオートファジーの関係を明らかにすることを目的として研究を行いました。
研究の手法と成果
ヒトの膵がん細胞としてよく使われているMIA PaCa-2細胞6)に放射線(6グレイのX線)を照射しました。すると、12時間後に細胞周期チェックポイント、特にG2/M期チェックポイントと呼ばれるDNA損傷と関係した監視装置のチェックポイントが活性化してG2期で細胞周期が止まり、それとほぼ同時にオートファジーの誘導が起こることがわかりました(図2)。一方、放射線を照射していない細胞では、G2期にある細胞でもオートファジーの誘導は起きておらず、細胞周期も次のM期に進んでおり、G2/M期チェックポイントは活性化していませんでした。
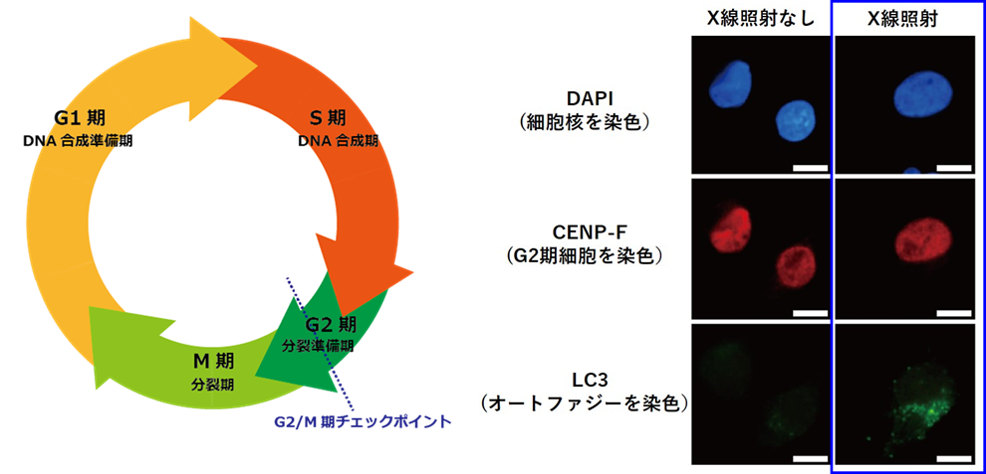
図2 X線照射したヒト膵がん細胞におけるオートファジーの誘導
ヒト膵がん細胞(MIA PaCa-2細胞)にX線(6グレイ)を照射して12時間後の写真(青枠内)では、細胞周期がG2期の細胞(写真では赤)でオートファジー(写真では緑)が働いていており、細胞周期も止まったままだった。一方、X線を照射していない細胞の中にもG2期の細胞はあるが、オートファジーは働いておらず、細胞周期は次のM期に進んでいた。
この結果は、細胞周期を同調させて、細胞集団の内80%ほどの細胞がG2期にある状態で行っても同じだったことから、細胞がG2期にあるだけでオートファジーが起こるわけではなく、放射線照射による細胞周期チェックポイントの活性化に依存してオートファジーが誘導されると結論づけました。
そこで、MIA PaCa-2細胞をG2/M期チェックポイントの活性化を阻害する薬剤であるMK1775で処理した後に放射線を照射しました。その結果、薬剤で処理していない細胞と比べて増殖が抑制されたことから、放射線抵抗性が減少していることが示されました(図3)。
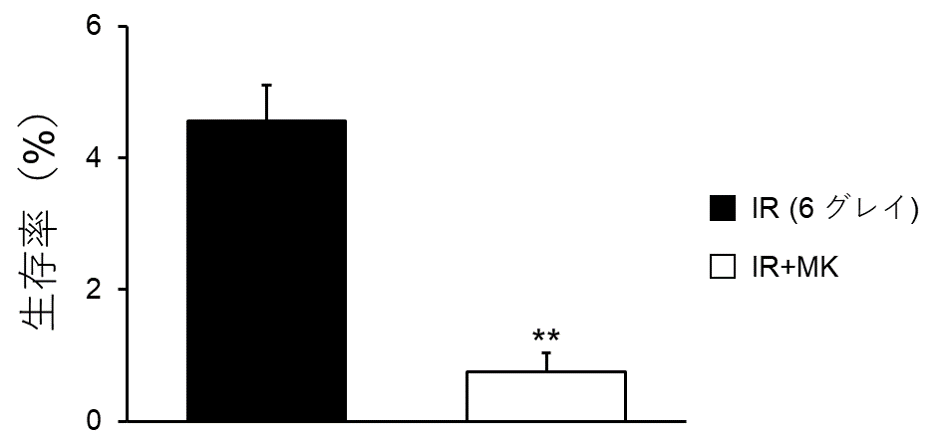
図3 X線とG2期チェックポイント阻害剤を併用した際の細胞生存率の比較
ヒト膵がん細胞(MIA PaCa-2)に6 グレイのX線照射単独(IR)、またはX線とG2期チェックポイント阻害剤(IR+MK)を併用した際の細胞生存率を比較した。X線単独に比べてG2期チェックポイント阻害剤を併用した方の細胞では生存率が低く、すなわち放射線の治療効果が阻害剤により増強された。
さらに、ヒト膵がんモデルマウスにMK1775を投与して放射線(3グレイのX線)治療を行いました。その結果、膵がんのサイズ増加が抑制されました(図4)。
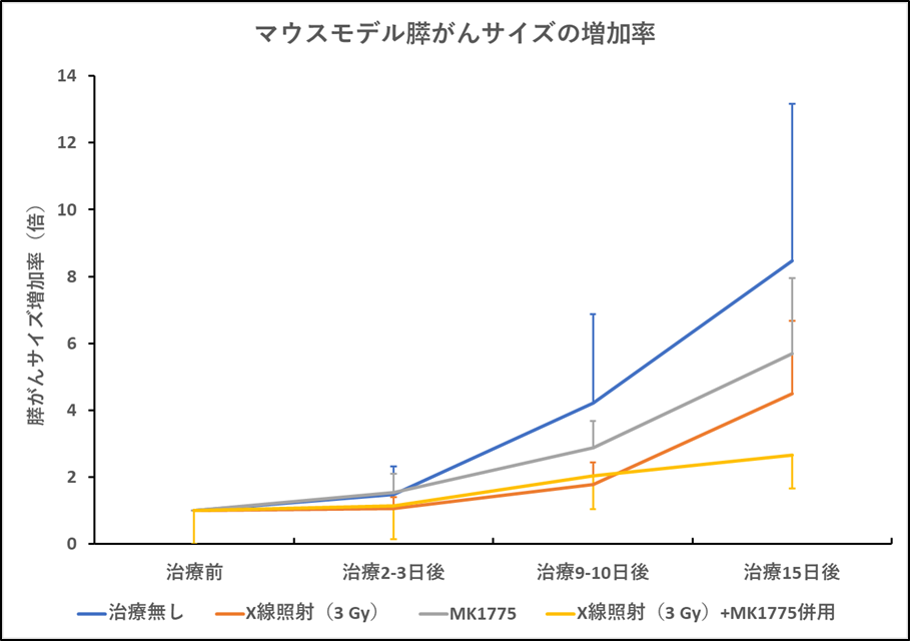
図4 G2チェックポイント阻害薬剤と放射線(X線照射)治療の併用によるがん増殖抑制効果の比較
治療(X線照射あるいはG2チェックポイント阻害薬剤)無し、X線照射のみ、G2チェックポイント阻害薬MK1775のみ、X線照射とMK1775併用の各群でMIA PaCa-2細胞を皮下移植したマウスにおけるがん増殖効果を比較した。X線照射とMK1775の併用治療により、治療開始15日目では他のグループに比べて膵がんの増加率が低く抑えられた(黄色線)。
今後の展開
本成果により、膵がんの放射線治療に対する抵抗性のメカニズムの一端が明らかになりました。膵がん細胞での放射線治療抵抗性メカニズムを薬剤等で阻害することにより、放射線治療の効果が高まることも明らかとなりました。今後、膵がんに対する放射線治療効果を増感する方法開発に繋がることが期待されます。
用語解説
1)細胞周期チェックポイント
一つの細胞が二つの娘細胞へと分裂する過程(細胞周期)において、その過程に発生した異常(損傷など)を感知して細胞周期を一時的に止める機構。細胞周期が停止している間に異常を修復することで娘細胞に異常が伝わらない様にしている。
2)オートファジー
細胞が自己成分(タンパク質や細胞内小器官など)を分解する機構。自己成分の分解により、飢餓状態では細胞生存に必要な生体分子を作り出す働きの他に、細胞内の不要物を分解して新陳代謝も担う。このためオートファジーの機能不全は様々な疾患につながる。
3)量子メス
量研が研究開発中の小型で高性能な重粒子線がん治療装置。量研が持つ高強度レーザー技術と超伝導技術の応用により、既存の病院建物内に設置できる×にまで小型化し、炭素だけでなく、酸素、ヘリウムを組み合わせたマルチイオン照射装置を備えることにより、より効果的な照射、副作用の低減、照射回数の減少を実現することを目指している。
4) G2/M期チェックポイント
細胞周期の進行を制御する機構の一つで、細胞がゲノムDNAの損傷を持ったまま有糸分裂(M期)に入るのを防ぐ。この部位に異常があるとDNA修復が行えず細胞が癌化する原因となるため、癌治療における標的の一つとなっている。
5) ATP
全ての動物や植物の細胞内に存在するエネルギー分子。細胞はをとリン酸に加水分解することで生まれるエネルギーによって活動している。
6) MIA PaCa-2細胞
ヒト膵管腺癌細胞株。白人男性の膵がん組織から採取された。倍加時間は時間で、広く実験細胞として使用されている。
