発表のポイント
- 蛍光ナノダイヤモンドは、細胞イメージングや極微量ウイルス検出などにおける高感度の蛍光標識剤として注目されている。
- レーザー光による量子操作で蛍光ナノダイヤモンドの検出効率を大幅に向上させ、信号/背景光比が従来よりも100倍以上高い超高感度蛍光イメージング技術の開発に世界で初めて成功した。
- 細胞や生体の高感度イメージングだけではなく、ウイルス感染症等の早期・迅速診断、認知症やがんなどの早期診断を実現する「量子診断プラットフォーム」への活用が期待される。
- 特殊な機材を使用せず、低出力レーザーのシンプルな制御のみで超高感度検出が達成された。医療分野、産業分野における装置化を目指す。
国立研究開発法人量子科学技術研究開発機構(理事長 平野俊夫)量子生命・医学部門量子生命科学研究所次世代量子センサーグループの五十嵐龍治グループリーダー、柳瑶美博士研究員、神長輝一研究員らは、群馬大学(学長 石崎泰樹)の花泉修教授、加田渉准教授らと共同で、細胞イメージングや極微量ウイルス検出などへの活用が期待される蛍光ナノダイヤモンド1)の検出効率を大幅に向上する新規イメージング手法の開発に成功しました。
蛍光を用いた生体イメージング技術は生命現象の解明に広く用いられています。また、ウイルス検査などの臨床検査等においても、蛍光検出は重要な基礎技術です。しかし、自家蛍光2)など望ましくない位置にも発光が観察される「背景光」の存在により、偽陽性などの誤った結果がもたらされる場合があります。本研究グループは、窒素-空孔中心(NVセンター3))と呼ばれる原子配列の乱れを含むナノサイズの蛍光ダイヤモンド(蛍光ナノダイヤモンド)を蛍光試薬として使用し、レーザー光による量子操作4)を行いながら蛍光検出することで、背景光の影響を排除した超高感度蛍光イメージング技術を開発しました(特願2021-104440、104441(日本))。一般的な蛍光イメージングと比較して、高い背景光排除効果を発揮し、信号/背景光比(SBR値、後述)にして100倍以上の性能向上に成功しました。
今回開発した手法の活用により、細胞内にわずかしか存在しない分子であっても特異的かつ高感度に検出することが可能です。これまで観察できなかった少数分子の機能の解明や、病態に及ぼす影響の解析に役立つと考えられます。また、ウイルスを超高感度で検出する技術として近年注目される「量子診断プラットフォーム5)」にも、この技術をそのまま利用でき、ウイルス感染症の早期・迅速診断技術としての社会実装も期待できます。
本研究は、JST戦略的創造研究推進事業 さきがけ「コンポジット量子センサーの創成 -1細胞から1個体まで」(JPMJPR18G1)、さきがけ「ナノダイヤモンドによる三次元構造動態イメージング技術の創成」(JPMJPR14F1)および文部科学省 光・量子飛躍フラッグシッププログラム(Q-LEAP, JPMXS0120330644)、および官民研究開発投資拡大プログラム(PRISM, JP19gm6110022h001)の支援を受けています。また、MEXT/JSPS科研費(JP20H02587, JP20H00453, JP18H06501, JP20K19969, JP18K11916, JP18K18839, JP17H01262)の支援も受けています。また、部分的に文部科学省 光・量子飛躍フラッグシッププログラム(Q-LEAP, JPMXS0118067395)における開発技術も使用しています。この研究成果はこの分野においてインパクトの大きい論文が数多く発表されている米国化学会発行の「ACS Nano」のオンライン版に2021年8月3日(火曜日)に掲載されました。
研究の背景
蛍光を用いた生体イメージングは、生命科学や臨床医学においてさまざまな場面で活用される重要な技術であり、細胞や生体内の分子局在やその機能の解析において、今や欠かせない技術となっています。また、病理診断6)やウイルス検査の際にも、蛍光検出に基づく蛍光抗体法7)やリアルタイムPCR法8)等が広く活用されています。蛍光検出は他の検出技術と比べて非常に高感度で、ごく少数の細胞や分子(1細胞・1分子レベル)の検出に利用できます。その一方で、自家蛍光や夾雑物(きょうざつぶつ。不純物など余計な混ざりものの意)の蛍光など、観たい対象以外からの発光(背景光)が蛍光検出の妨げとなり、偽陽性9)などの誤った結果をもたらすことがあります(図1)。
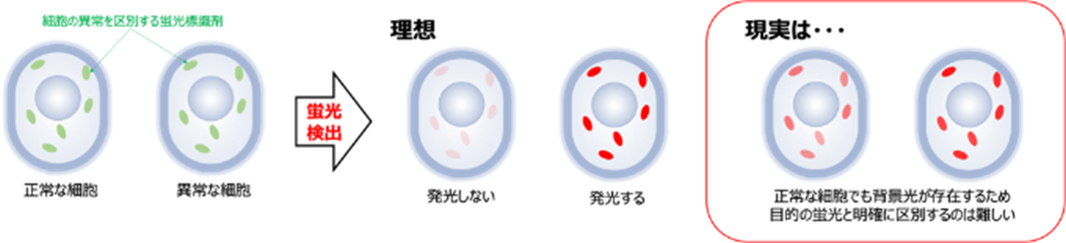
図1:蛍光検出による細胞イメージングの概要と背景光がもたらす影響
背景光に対して、観たい信号光がどのくらい効率的に取り出せているかを表す指標として、「信号/背景光比(SBR値)」が一般的に用いられています。SBR値は、「背景光の強さに対して、信号光が何倍の強さで検出されたか」を示す値です(図2)。SBR値が1を下回ると、信号光は背景光よりも弱く検出されたということになります。そしてSBR値が小さくなるにつれて、背景光から信号光を区別するのは次第に困難になります。また、実際の信号はノイズ(雑音)も含むので、偽陽性などを避けるためにはSBR値をできる限り高める必要があります。

図2:信号/背景光比(SBR値)。SBR値が高いほど文字が識別しやすいことがわかる。
ところが、ランダムに発生するノイズであれば計測時間を長く取ることで排除できますが、背景光は信号光とほぼ同じ性質を持つ発光であるため、計測時間を長く取っても取り除くことができません。このため、従来の蛍光観察技術でSBR値を高めるのには限界がありました。
研究の手法と成果
この背景光の問題を解決する方法として、責任著者の五十嵐は2012年に、蛍光ナノダイヤモンドを蛍光標識剤10)として活用し、ダイヤモンド結晶中の蛍光体である“NVセンター(図3a)”の量子操作を利用することで、背景光を高効率で排除するイメージング技術を開発しました[1]。この技術は近年、生きた培養神経細胞のイメージングや[2]、極微量のRNAウイルス11)の超高感度検出等を実現する「量子診断プラットフォーム[3], [4]」にも活用されています[5]。しかしこの方法は、マイクロ波で電子スピンの状態を操作する複雑なシステムが必要となるため、装置が高価で大型なものとなり、一般的な生物学研究や臨床検査現場への普及が進まない原因となっています。また、計測試料によってはマイクロ波の照射に伴う試料へのダメージが懸念される場合もありました。
そこで私たちは、マイクロ波を用いず緑色励起光の照射間隔の制御のみでNVセンターのスピン量子状態を操作し、背景光を排除して蛍光ナノダイヤモンドを選択的に検出する新たなイメージング技術を考案しました。この手法では、(1)長周期のレーザーパルス12)中では乱雑なスピン量子状態を、短周期のレーザーパルス中では秩序的なスピン量子状態を取る、(2)この秩序的なスピン量子状態では、乱雑なスピン量子状態と比較して蛍光強度が増強するという、NVセンターの性質を利用しています(図3b)。自家蛍光や夾雑物の蛍光のような背景光ではこの速さのレーザーパルス周期に依存した蛍光強度変化は起こらないため、秩序的なスピン量子状態の画像と乱雑なスピン量子状態の画像とで差分を取ることにより、蛍光ナノダイヤモンドから発する蛍光を選択的に取得し、画像化することが可能です(図3c)。
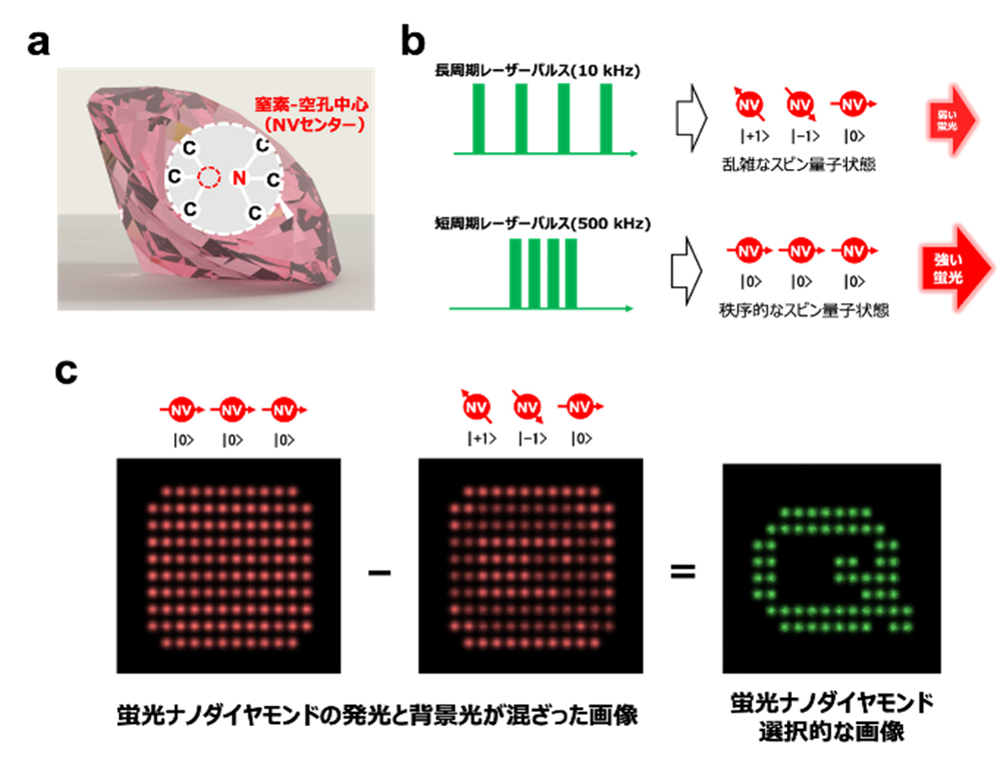
図3:(a)NVセンターの構造。(b)開発技術で利用したNVセンターの性質。(c)蛍光ナノダイヤモンド選択的な画像の取得方法。蛍光ナノダイヤモンドの輝点では短周期レーザパルス(左)よりも長周期レーザーパルス(中)では蛍光が弱くなる。蛍光ナノダイヤモンド以外の輝点ではそのような変化は起こらないので、これらの差分を得ることで背景光の影響を受けずに蛍光ナノダイヤモンドのみ選択した画像(右)が得られる。
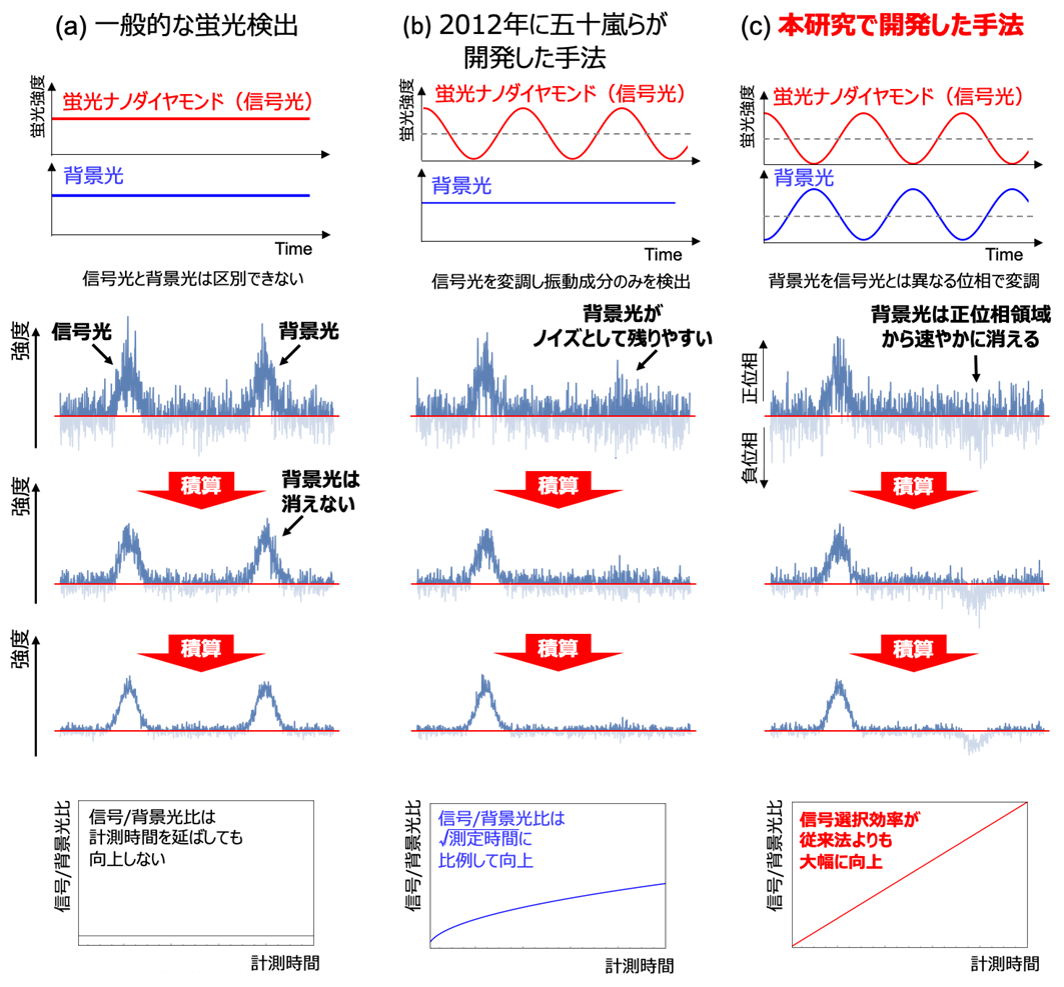
図4 従来法と本研究で開発した手法との比較。(a)一般的な蛍光検出では蛍光ナノダイヤモンドの発光(信号光)と背景光は区別できないため、計測時間を延ばして信号品質(画質)を高めてもSBR値は向上しない。(b)2012年に責任著者の五十嵐らが開発した方法[1](特許第5476206号)では、信号光にのみ強度変調をかけることで、変調の有無で信号光と背景光を区別した。その結果、計測時間を延ばせば延ばすほど背景光は取り除かれ、信号光が増幅されるといった効果が得られた。ただし、背景光はノイズも強めるため、背景光の除去効率は不十分だった。(c)本研究で開発した手法では、さらに背景光にも別の強度変調を与えることで、信号光と背景光をより区別しやすくすることに成功した(特願2021-104440、104441(日本))。これにより、2012年に開発した技術よりも圧倒的に短時間で効率的にSBR値を向上させることができるようになった。
量子操作を用いたこの手法に光学的手法と画像解析手法を組み合わせることで、蛍光ナノダイヤモンドの検出効率は劇的に向上し(図4)、一般的な蛍光イメージングと比較して信号/背景光比が100倍以上にもなることを確認しました。これはマイクロ波による量子操作を用いた従来の選択イメージング技術と比較しても1桁以上の大幅な検出効率の向上となります。
また、蛍光ナノダイヤモンドを培養細胞や線虫(C. elegans)13)、ラットの海馬14)などに導入し、開発した技術をさまざまな生体試料に対して適用することで、その有用性を示しました。図5はその一例です。蛍光染色したミトコンドリア15)の強い背景光の影響を受けずに、培養細胞中に導入した蛍光ナノダイヤモンドを選択的にイメージングできることを示しました。
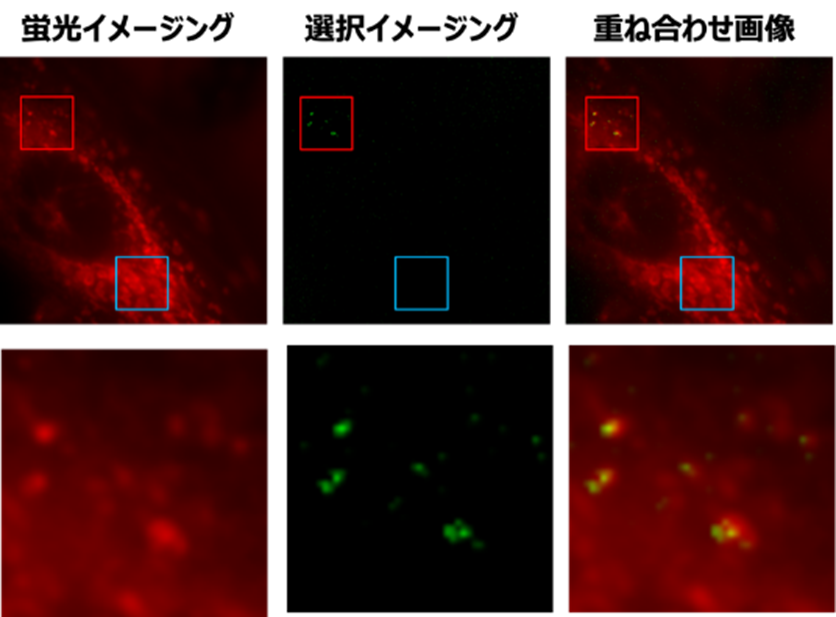
図5 開発技術による培養細胞内での蛍光ナノダイヤモンドの選択イメージング。緑は蛍光ナノダイヤモンド、赤は蛍光染色したミトコンドリア。ミトコンドリア染色に使用した蛍光分子と蛍光ナノダイヤモンドは同一の蛍光波長帯で発光し、通常の蛍光イメージングでは区別することができない。上段の赤枠内は蛍光ナノダイヤモンドが存在する部位、青枠内は蛍光ナノダイヤモンドが存在しない部位。下段は上段の赤枠内の拡大図。
今後の展開
本研究で開発した技術により背景光の影響を排除して、蛍光ナノダイヤモンドを極めて高効率かつ高感度で検出できるようになりました。このことは、生命科学研究における蛍光イメージング技術の改善だけではなく、PCR法によるウイルス検査の大幅な高感度化による精度向上、高速化の実現にもつながります。実際に、蛍光ナノダイヤモンドを利用することで分子検出感度が従来技術の10万倍向上し、感染初期の段階でヒト免疫不全ウイルス(HIV;新型コロナウイルスと同じRNAウイルスの一種)を検出できることが知られています[3-5]。
本研究で開発した技術は、従来必要とされたマイクロ波が不要であるためシステムが大幅に簡便になり、安価で小型な装置の実現も可能です。従って、生物学研究や臨床検査現場への普及が進むと考えられます。また、ウイルス感染症だけではなく、この技術により血液などに存在する微量のバイオマーカー16)分子の高感度検出が可能となれば、認知症やがんの早期診断法としても社会実装されることが期待できます。
用語解説
1)蛍光ナノダイヤモンド
おおよそ100ナノメートル以下のダイヤモンドをナノダイヤモンドと呼ぶ。研究や工業分野などでは人工的に作られたダイヤモンドが用いられる。化学構造は宝飾品として用いられる天然のダイヤモンドと全く同じだが、人工ナノダイヤモンドは非常に安価なため、研磨剤やエンジンオイルの添加剤、鉛筆の芯の潤滑剤などとしても幅広く利用されている。その中でも、結晶中にNVセンター(後述)の構造を持つようなナノダイヤモンドは、赤色の蛍光を発することから「蛍光ナノダイヤモンド」と呼ばれる。
2)自家蛍光
細胞内や生体内に元から存在する生体分子に由来する蛍光。人為的に加えられた蛍光マーカーに由来する蛍光と区別してこのように呼ばれる。自家蛍光は広い波長域に存在するため、実験や診断においては自家蛍光を蛍光マーカー由来の蛍光と誤認し、誤った結論を導くことのないように細心の注意が求められる。
3)NVセンター
ダイヤモンド結晶中の不純物窒素(Nitrogen)と、その隣に形成された空孔(Vacancy)が作る原子配列の乱れ・欠陥。NVセンターは周辺環境の変化に極めて敏感に検知して量子状態が変わる特性があり、この特性をセンサとして利用できる。このため、NVセンターを持つダイヤモンドは「量子センサ」と呼ばれて注目されている。本研究のNVセンター作成は量子科学技術研究開発機構高崎量子応用研究所の電子線照射施設において行われた。
4)量子操作
スピン量子状態などの量子状態を定常状態とは異なる状態に人為的に変化させる技術。例えば、定常状態でNVセンターなどの電子スピンは方向が揃っておらず乱雑な向きを持つが、一定の緑色光を照射することで向きが揃った秩序的な状態を取ることが知られている。
5)量子診断プラットフォーム
NVセンターによる量子センシングを用いた疾患や感染症などの超高感度診断技術。金ナノ粒子を用いた高感度の診断技術と比較しても5桁優れた感度で分子検出が可能であり、HIV-1感染の初期段階で採取された試料においてRNA(ribonucleic acid:リボ核酸)ウイルス由来のRNAが検出できることが示されている。このため、同じRNAウイルスであるSARS-CoV-2を原因ウイルスとする新型コロナ感染症の迅速診断への活用も期待されている。
6)病理診断
患者から採取された組織などの試料を顕微鏡で観察することにより、病変の有無や種類、病気の程度などを評価する診断方法。
7)蛍光抗体法
蛍光色素によって標識した抗体を用いることで組織標本を染色し、蛍光顕微鏡などで抗原の分布を調べる組織学的手法。
8)リアルタイムPCR法
PCR(polymerase chain reaction:DNAポリメラーゼ連鎖反応)の増幅量を蛍光検出によりリアルタイムでモニターする迅速、高感度かつ定量的なPCR解析手法。現在、新型コロナウイルスの検出方法としてリアルタイムPCR法の一種であるリアルタイムRT-PCRが採用されている。
9)偽陽性
実際には病気にはかかっていないにもかかわらず検査で陽性の結果が出ること。逆に病気にかかっているにもかかわらず検査で陰性の結果がでることは「偽陰性」と呼ぶ。あらゆる病気の診断技術は感度や特異度が100%ではないため、一定数の偽陽性や偽陰性が生じる。
10)蛍光標識剤
特定の化学構造と反応する活性を持つ蛍光分子。免疫染色やフローサイトメトリーによる細胞情報の解析においては蛍光標識材によりタンパク質が標識される。
11)RNAウイルス
RNAを遺伝情報として持つウイルスの総称。後天性免疫不全症候群の原因ウイルスであるHIVや、新型コロナウイルス感染症の原因ウイルスであるSARS-CoV-2は、いずれも1本鎖のRNAを遺伝情報として持ち、RNAウイルスとして分類される。
12)レーザーパルス
短い時間だけ照射されるレーザー光。
13)線虫(C. elegans)
体長1ミリメートル程度の多細胞生物で、2002年ノーベル生理学・医学賞の「プログラム細胞死」(シドニー・ブレナー)、2006年ノーベル賞生理学・医学賞受賞の「RNA干渉」(アンドリュー・ファイア、クレイグ・メロー)、2008年ノーベル化学賞受賞の「緑色蛍光たんぱく質」(マーティン・チャルフィ)にも用いられた優れたモデル生物として知られる。特に近年、C. elegansの栄養状態と寿命との密接な関係が明らかになり、老化研究の優れたモデル系として期待されている。
14)海馬
脳内の大脳辺縁系にある海馬体の一部で、脳の記憶や空間認識に関係する器官。アルツハイマー病においては海馬が早期に傷害されることが知られている。
15)ミトコンドリア
細胞の呼吸によって、生命を維持する活動を行うのに必要なエネルギーを取り出すための細胞小器官。その役割から「細胞のエネルギー工場」とも称される。
16)バイオマーカー
特定の疾病のリスクや進行の度合いの目安となる生理学的な指標。ここでは特に、血液や鼻腔ぬぐい液などで測定されるタンパク質等の生体分子を意味する。
掲載論文情報
Tamami Yanagi, Kiichi Kaminaga, Michiyo Suzuki, Hiroshi Abe, Hiroki Yamamoto, Takeshi Ohshima, Akihiro Kuwahata, Masaki Sekino, Tatsuhiko Imaoka, Shizuko Kakinuma, Takuma Sugi, Wataru Kada, Osamu Hanaizumi* and Ryuji Igarashi* (*は責任著者)
“All-optical Wide-field Selective Imaging of Fluorescent Nanodiamonds in Cells, in Vivo and ex Vivo”
Acs Nano (2021)
https://pubs.acs.org/doi/10.1021/acsnano.0c07740
参考文献
[1] R. Igarashi et al., “Real-Time Background-Free Selective Imaging of Fluorescent Nanodiamonds in Vivo,” Nano Letters, vol. 12, no. 11, pp. 5726–5732, Nov. 2012.
[2] D. A. Simpson et al., “Non-Neurotoxic Nanodiamond Probes for Intraneuronal Temperature Mapping,” Acs Nano, vol. 11, no. 12, pp. 12077–12086, Dec. 2017.
[3] “生物工学:ナノダイヤモンドを用いた量子診断プラットフォーム,” 2020. [Online]. Available: https://www.natureasia.com/ja-jp/nature/highlights/105618.
[4] “生物工学:超高感度診断向けのスピン増強ナノダイヤモンド・バイオセンシング,” 2020. [Online]. Available: https://www.natureasia.com/ja-jp/nature/587/7835/s41586-020-2917-1/超高感度診断向けのスピン増強ナノダイヤモンド・バイオセンシング.
[5] B. S. Miller et al., “Spin-enhanced nanodiamond biosensing for ultrasensitive diagnostics,” Nature, 2020.
