発表のポイント
- 中皮腫1)細胞に結合してα線2)を放出する標的アイソトープ治療3)薬候補アクチニウム225(225Ac)標識抗ポドプラニン抗体4)を、中皮腫モデルマウスに投与して、がんサイズの縮小効果と生存期間延長を確認しました。
- 既存の治療法では効果がない悪性中皮腫に対する新たな治療法となることが期待されます。
国立研究開発法人量子科学技術研究開発機構(理事長 平野俊夫。以下「量研」という。)量子生命・医学部門量子医科学研究所分子イメージング診断治療研究部の須藤仁美主任研究員、辻厚至グループリーダー、東達也部長は、国立大学法人東北大学大学院医学系研究科の加藤幸成教授、金子美華准教授と共同で、悪性中皮腫(がん)に対するα線放出核種を用いた治療薬候補の開発に成功し、動物実験によりその抗がん効果を明らかにしました。
中皮腫は、胸膜、腹膜などにある中皮から発生する悪性腫瘍で、80-85%が胸膜から発生します。中皮腫の原因のほとんどは、アスベストばく露です。2005年のクボタショック5)を契機に大きな社会問題となりました。日本国内における悪性中皮腫による死亡者数は増加の一途をたどっています。アスベストの輸入及び使用量は1970〜1980年代がピークで、2004年に全アスベストに対して原則使用禁止となりましたが、アスベストばく露から発症までの潜伏期間が25〜50年とされていることから、悪性中皮腫の発生ピークは2030年頃、罹患者数は年間3,000人に及ぶと予測されています。診断される患者の7割以上が進行がんであり、有効な治療法がなく予後が悪いため、新たな治療法が望まれています。
量研では、放射線の飛ぶ距離が細胞数個分と短く、当たった細胞を殺傷する能力が高いα線を放出する核種225Acを加速器で効率よく製造することに成功しています。225Acは、近年、前立腺がん特異的膜抗原(PSMA)を標的とした前立腺がんで注目されている標的アイソトープ治療用の放射性同位体です。
この225Acを中皮腫細胞だけに届けることが出来れば、飛距離の短いα線により、周囲の正常細胞を傷つけることなく、効率よくがん細胞を殺傷することが可能です。そこで、本研究チームは、中皮腫細胞の細胞表面に多く存在しているポドプラニン6)というタンパク質に結合する抗体NZ-16(以下、「NZ-16」という。」)を225Acで標識し、α線標的アイソトープ治療薬候補として225Ac標識NZ-16を開発しました。ポドプラニンは中皮腫の中でも特に悪性度の高い肉腫型でも高発現しているタンパク質で治療標的として有望です。
225Ac標識NZ-16を中皮腫のモデルマウスに1回投与したところ、腫瘍サイズを縮小させ、腫瘍をほぼ消失させる効果があることを確認しました。また、生存期間を延長させることも確認しました。一方で、副作用の指標となる体重減少や病理所見は認められませんでした。更に、α線と同様にがん細胞殺傷能力を有するβ線7)を放出する放射性同位体イットリウム90(90Y)を付加した90Y標識NZ-16と225Ac標識NZ-16の抗腫瘍効果を比べたところ、225Ac標識NZ-16は90Y標識NZ-16よりも高い腫瘍縮小効果があることを確認しました。これらの研究成果から、悪性中皮腫に対して、225Ac標識NZ-16によるα線標的アイソトープが副作用の少ない効果的な治療法となることが期待されます。現在、臨床応用に向けて関係機関と協力して準備を進めており、3年後のFirst-in-human試験の実施を目指しています。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)「橋渡し研究プログラム」シーズB、および橋渡し研究支援拠点(東北大学)の支援により実施した成果を一部活用したもので、「Cells」(インパクトファクター6.6)2021年9月22日にオンライン掲載されました。
研究の背景と目的
中皮腫は、胸膜、腹膜などにある中皮から発生する悪性腫瘍で、80-85%が胸膜から発生します。中皮腫の原因のほとんどは、アスベストばく露です。2005年のクボタショックを契機に、大きな社会問題となりました。日本国内における悪性中皮腫による死亡者数は1995年の500人から、2000年710人、2005年911人、2015年1,504人、2017年1,555人 と確実に増加の一途をたどり、世界全体では年間4万人が死亡しています。アスベストの輸入及び使用量は1970〜1980年代がピークで、2004年に全アスベストに対して原則使用禁止となりましたが、アスベストばく露から発症までの潜伏期間が25〜50年とされていることから、日本では悪性中皮腫の発生ピークは2030年頃、罹患者数は年間3,000人、アスベスト使用禁止が遅れている先進国の一部と開発途上国でも患者の増大が予測されています。
診断される患者の7割以上が進行がんであり、外科療法、内科療法、放射線療法を組み合わせた最新の治療が行われていますが、有効な治療法がなく予後が悪いため、新たな治療法が望まれています。しかし、罹患率は日本国内で900人/年と患者が少ない、いわゆる希少がんであるため、民間企業による開発は活発ではなく、アカデミア主体での開発が必要な状況です。
量研は、放射線の飛ぶ距離が細胞数個分と短く、当たった細胞を殺傷する能力が高いα線を出す核種225Acを加速器で製造することに成功しています。この225Acを中皮腫細胞に効率よく届けることが出来れば、飛距離の短いα線により、周囲の正常組織に障害を与えることなく中皮腫を治療することが可能ではないかと研究チームは考えました。
225Acを中皮腫細胞に届ける手法として、中皮腫細胞の表面に高率に存在しているポドプラニンタンパク質に着目しました(図1)。ポドプラニンは、がんの悪性度にも関係しており、治療抵抗性の中皮腫細胞の治療標的分子として有望です。ポドプラニンを認識する抗体に225Acを結合すれば中皮腫細胞に届けられると考えられます。ところが、ポドプラニンはリンパ管内皮細胞にも存在しており、この細胞に225Acが届いてしまうと重篤な副作用が生じると懸念されていました。そこで本研究では、東北大学が開発した正常組織のポドプラニンを認識せず、腫瘍に発現しているポドプラニンだけを認識する抗体NZ-16を用いて、その抗体に225Acを付加した225Ac標識NZ-16を開発し、中皮腫に対する抗腫瘍抑制効果をモデル動物において評価しました。
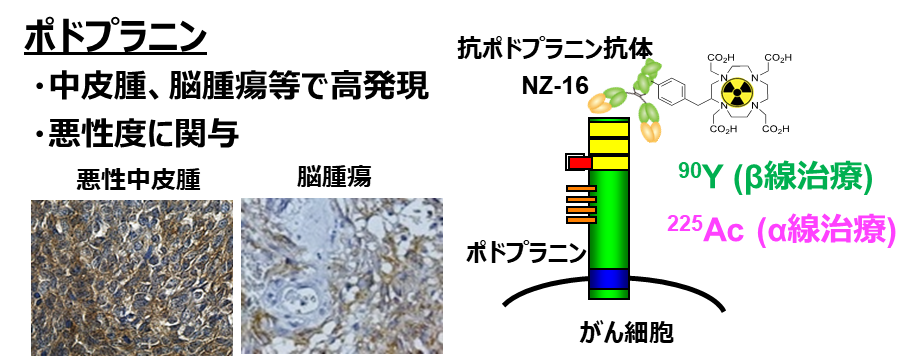
図1. ポドプラニン及び放射性標識抗体
ポドプラニンは、細胞膜表面に存在するタンパク質です。中皮腫、脳腫瘍
などで高発現しており、その悪性度に関与しています。本研究では抗ポドプ
ラニン抗体NZ-16を、α線放出核種アクチニウム225(225Ac)やβ線放出核種イ
ットリウム90(90Y)で放射性標識し、中皮腫モデルマウスで治療効果を評価しました。
研究の手法と成果
α線標的アイソトープ治療薬候補として、225AcをNZ-16抗体に結合させた225Ac標識NZ-16を作製しました。α線とβ線の治療効果を比較するため、β線放出核種90YをNZ-16抗体に結合させた90Y標識NZ-16も作製しました。
中皮腫細胞を皮下に移植した中皮腫モデルマウスにNZ-16単体、90Y標識NZ-16および225Ac標識NZ-16をそれぞれ1回静脈投与して、腫瘍の大きさとモデルマウスの生存期間について56日間観察しました。
その結果、225Ac標識NZ-16は18.5kBq (キロベクレル8))の投与で、90Y標識NZ-16の3.7MBq (メガベクレル)の投与と比べて、有意ながん増殖抑制効果が確認されました(図2)。この違いは、225Acから放出されるα線のエネルギーが大きいことに加え、細胞殺傷効果が高いことによるものです。225Ac標識NZ-16の効果は観察期間中持続し、再増殖は観察されませんでした(図2)。生存期間については、225Ac標識NZ-16の延長効果が高かく、観察期間最終日で225Ac標識NZ-16では100%の処置マウスが生存し、90Y標識NZ-16では60%でした(図3)。また、副作用として懸念された体重減少や病理変化は観察されませんでした(図4)。
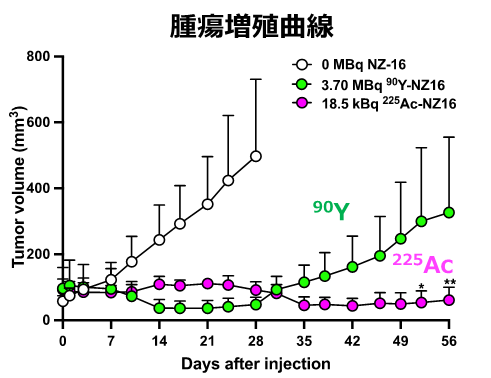
図2. 治療効果
左図は、抗体投与後の腫瘍サイズの変化を示しています。白丸はNZ-16抗体
単独、緑の丸は90Y標識NZ-16 (3.7MBq)、ピンクの丸は225Ac標識NZ-16
(18.5kBq)投与群(各群N=5)の結果。右図は、各処置群の代表的なマウスの画像。
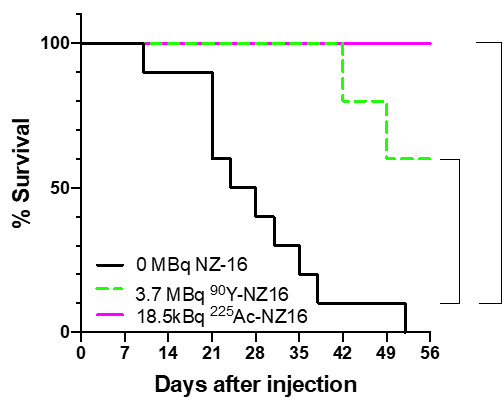
図3.生存曲線
抗体投与後の生存率を示している。黒線はNZ-16単独、緑の線は90Y標識NZ-16 (3.7MBq)、
ピンクの線は225Ac標識NZ-16 (18.5kBq)投与群(各群N=5)の結果。
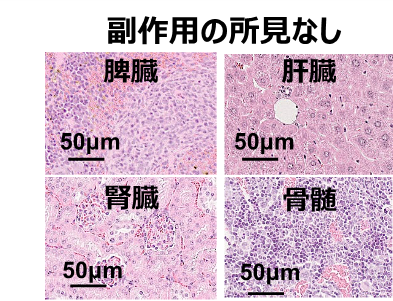
図4. 225Ac標識NZ-16投与マウスの病理像
225Ac標識NZ-16を投与したマウスの主な臓器のヘマトキシリン・エオジン染
色像。副作用の所見は認められませんでした。
今後の展開
本成果により225Ac標識NZ-16抗体によるα線標的アイソトープ治療は、既存の治療が効かない中皮腫に対する副作用の少ない、効果的な治療法となることが期待されます。現在、AMED橋渡し研究プログラムの支援を受けて、臨床試験に必要な非臨床試験計画の策定を進めております。現在、臨床応用に向けて関係機関と協力して準備を進めており、3年後にFirst-in-human試験の実施を目指しています。
用語解説
1)中皮腫
中皮腫は胸膜や腹膜をおおっている膜を構成している細胞のひとつ中皮細胞が悪性化したもので、発生部位は胸膜(80~85%)、腹膜(10~15%)、心膜(2%程度)、精巣鞘膜(1%以下)にみられます。発症原因は、欧米男性悪性中皮腫症例の78〜88%で、女性の23〜65%でアスベスト(石綿)ばく露との関連性が指摘されています。アスベストの取り扱い実態を見ると、輸入及び使用量は1970〜1980年代がピークでしたが、使用規制として含有率1%超について輸入・使用禁止となったのは1995年であり、全アスベストに対して原則使用禁止とされたのは2004年です。このような規制の遅れによる健康被害の救済に石綿健康被害救済法が制定されています。罹患率は日本国内で900人/年と低く、いわゆる希少がんですが、世界的な罹患率は先進国(日本を含む)で10,000人/年、中国は2,000人/年となっています。また死亡者数も世界全体で年間4万人が死亡しており、アスベスト使用禁止が遅れている先進国の一部と開発途上国は患者の増加が予測されています。
2)α線
α線はヘリウム(He)原子核が非常に速いスピードで飛んでいるものです。物質中を通過する際、物質と相互作用し、例えば物質中の分子が持っている電子を弾き飛ばします(電離といいます)。α線(He原子核)は質量が大きく、物質中の分子などと衝突しやすいため、透過性が非常に低く、紙一枚で遮断することができる代わりに、物質中では短い通過距離で高いエネルギーを付与することから、分子などを密に電離することができます。α線を細胞に照射した場合、DNAに修復することが難しいキズ(DNA二重鎖切断)ができます。この現象はα線が、がん細胞を効果的に殺滅できる理由のひとつです。
3) 標的アイソトープ治療
細胞傷害能力を有する粒子放射線(α線やβ線)を放出する放射性同位体を用いた治療法。RI内用療法、核医学治療とも呼ばれます。がん細胞だけを標的とするように、がん細胞に集積する性質を持たせた放射性同位体を体内に注射し、がん細胞に粒子放射線を体内から照射し殺傷します。
4) 225Ac標識抗ポドプラニン抗体NZ-16 (225Ac標識NZ-16)
α線を放出する核種であるアクチニウム225(225Ac)で抗ポドプラニン抗体NZ-16を標識した放射性抗体医薬品候補です。NZ-16抗体は、中皮腫や脳腫瘍などで高発現しているポドプラニンタンパク質に結合する抗体で、東北大学で開発されました。ポドプラニンタンパク質は、細胞の表面に存在するタンパク質で中皮腫に対する新規治療薬開発の標的分子の候補です。
5)クボタショック
大手機械メーカーであるクボタから公表されたアスベスト(石綿)による健康被害のこと。同社の旧工場の従業員および工場周辺住民がアスベストによって中皮腫等の関連疾病の被害を受けました。
6)ポドプラニン
ポドプラニンは、細胞表面に存在し、細胞の増殖や分化などに関与しているタンパク質です。中皮腫や脳腫瘍などで高い発現がみられ、発現の程度はがんの悪性度と関連があることが報告されています。
7)β線
β線は電子が非常に速いスピードで飛んでいる放射線の一種です。放射性同位体の原子核から放出されるβ線もα線同様にDNAにキズをつけますが、α線に比べると修復しやすいキズをつけると言われており、その細胞殺傷効果はα線に比べると低いとされています。
8)Bq(ベクレル)
Becquerelの略で、1秒間に崩壊する原子の個数を表す放射能の単位です。
論文について
Preclinical Evaluation of Podoplanin-Targeted Alpha-
Radioimmunotherapy with the Novel Antibody NZ-16 for Malignant Mesothelioma
Hitomi Sudo 1, Atsushi B. Tsuji 1, Aya Sugyo 1, Mika K. Kaneko 2, Yukinari Kato 2,3, Kotaro Nagatsu 4, Hisashi Suzuki 4 and Tatsuya Higashi 1
1 Department of Molecular Imaging and Theranostics, Institute for Quantum Medical Science (iQMS), National Institutes for Quantum and Radiological Science and Technology (QST), 4-9-1 Anagawa, Inage, Chiba 263-8555, Japan
2 Department of Antibody Drug Development, Tohoku University Graduate School of Medicine, 2-1, Seiryo-machi, Aoba-ku, Sendai, Miyagi 980-8575, Japan
3 Department of Molecular Pharmacology, Tohoku University Graduate School of Medicine, 2-1 Seiryo-machi, Aoba-ku, Sendai, Miyagi 980-8575, Japan
4 Department of Advanced Nuclear Medicine Science, Institute for Quantum Medical Science (iQMS), National Institutes for Quantum and Radiological Science and Technology (QST), 4-9-1 Anagawa, Inage, Chiba 263-8555, Japan
