本件のポイント
- 特発性肺線維症注1は呼吸器疾患の中で最も予後不良な疾患で、その発症および進行メカニズムは明らかになっていない。
- 吸入シリカ注2が肺線維症の肺内に多く蓄積していることで肺線維症が進行し、予後不良な転帰をもたらしていることを世界で初めて示した。
- 診断目的に手術で切除された特発性肺線維症患者さんの肺組織に含まれる元素の高感度分析を、in-air micro-PIXE(大気マイクロ粒子線励起X線分析)注3と呼ばれるイオンビーム装置を用いて行った
- コントロール(対照)肺と比較して特発性肺線維症の肺組織中にシリカが多く含まれている事を示した。
- 肺組織中のシリカが多ければ多いほど、肺線維症の進行のスピードが早いことが明らかになった。さらに、肺内のシリカの含有量が多い特発性肺線維症では、少ない症例と比較して生存期間が短かった。
- PM2.5や黄砂の研究ではシリカが主成分であることが報告されており1-3、環境因子の吸入が肺線維症の進行に関与している可能性が示唆される。
- 今後、肺へのシリカの吸入や蓄積を防ぐような予防医学が、肺線維症の発症や予後を改善させる可能性が期待される。
- 今回の報告は、あらゆる物質中の微量な元素成分を分析できるin-airmicro-PIXEを原因不明の難病の病態解明に応用した理工医の共同・連携研究である。
本件の概要
群馬大学大学院医学系研究科呼吸器・アレルギー内科学の古賀 康彦(こが やすひこ)助教らの研究グループは、量子科学技術研究開発機構高崎量子応用研究所上席研究員(佐藤 隆博、さとう たかひろ)と群馬大学大学院保健学研究科名誉教授(土橋 邦生、どばし くにお、現上武呼吸器内科病院院長)らとの共同研究により、難病疾患に指定されている特発性肺線維症(特発性間質性肺炎)の進行や予後に関わるメカニズムの一部を明らかにしました。
特発性肺線維症は、慢性的な経過で肺が硬くなってしまい、徐々に肺に空気が吸い込めなくなってしまう平均予後が3-5年と言われている難病です。治療法の開発が進む肺癌とは対照的に、肺線維症はその原因が特定できていないこともあって治療薬の開発が非常に遅れています。肺線維症は肺移植の対象疾患に指定されていますが、日本の肺移植待機期間は2-3年と欧米と比べてとても長いことから肺移植を待っている間に命を落とされてしまう患者さんがいらっしゃるのも現状です。現在、肺線維症の治療薬は2種類しかなく2015年以降は新薬が登場していないため、多くの肺線維症の患者さんが治療薬の開発を待ち望んでいらっしゃいます。
他臓器と大きく異なる肺組織の特徴は、外界と直接気道を介してつながっている事です。そのため研究者らは、外界からの何らかの刺激が肺線維症に関わりがあるのではないかと考えました。
そこで研究者らが着目したのが高崎量子応用研究所にあるin-air micro-PIXEと呼ばれる、物質に含まれる微量の含有元素の成分を検出できるイオンビーム分析装置でした。

研究者らは、in-air micro-PIXEを用いて肺内に微量に存在する元素の成分を測定し、肺線維症の病気のメカニズムの手がかりを見いだすことが出来ないかと考えました。
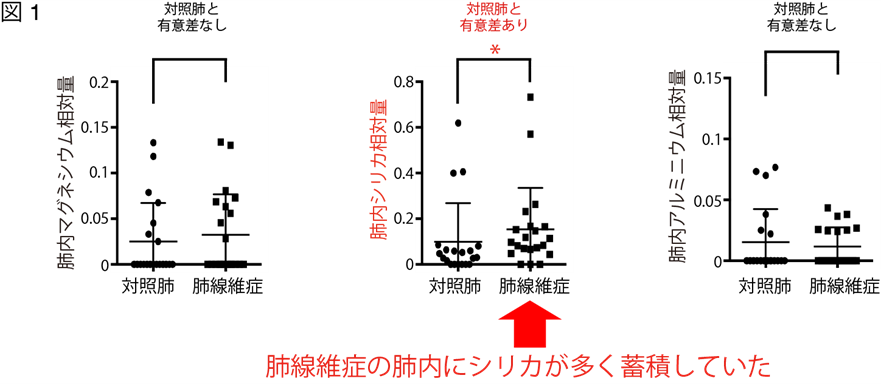
最初に、対照(コントロール)肺を早期肺癌の切除肺を用いて解析しました。早期肺癌手術では、肺癌を取り残さないようにその周囲の正常肺も一緒に切除します。その正常肺部分にイオンビームを照射して肺内に含まれている元素の成分を調べました。肺線維症の元素解析は、肺線維症の診断目的に手術で切除された肺組織を分析しました。その結果、対照肺と比較して肺線維症の肺内にシリカが多く蓄積していることがわかりました(図1)。
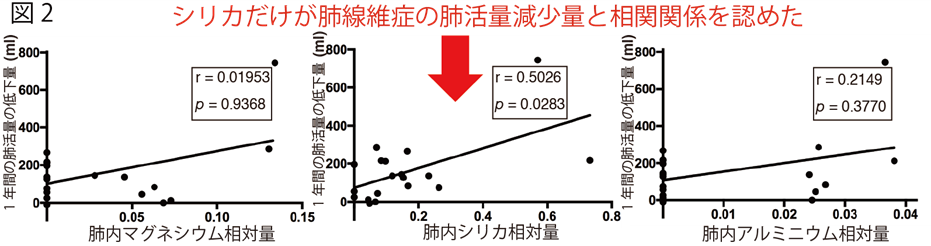
次に、肺線維症患者さんの肺活量の変化量を調べました。平均で150mLの肺活量が1年間で減少しており、従来の肺線維症の平均的な変化量と同じでした4, 5。なお健常者の1年間の肺活量の減少量は、約10-20mL前後です。
肺活量の減少は肺線維症の進行と比例します。つまり肺線維症が進行して肺が硬くなってくると肺活量も徐々に少なくなってきます。そこで1例1例の患者さんの肺内のシリカの量と肺活量の減少量とを比較分析したところ、肺内のシリカの量が多ければ多いほど肺活量の減少量が増えてしまっていることがわかりました(図2)。
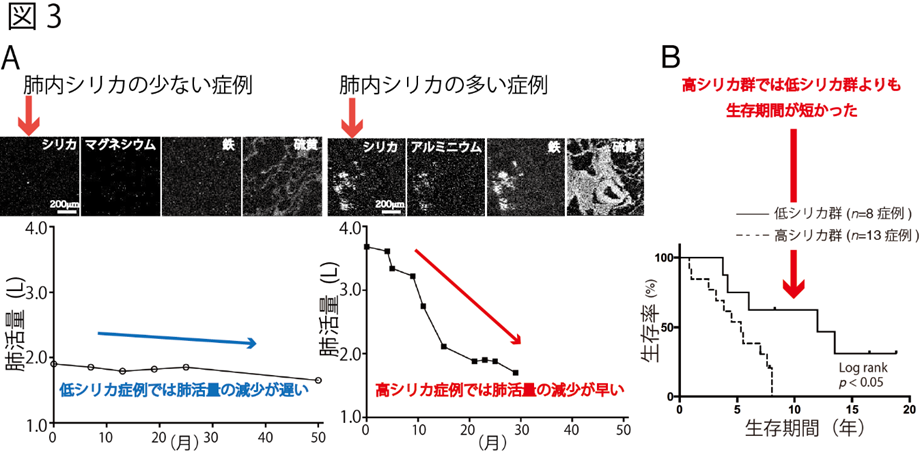
つまり肺内のシリカの量が多い患者さんは、肺線維症の進行が早いことが明らかになりました(図3A)。そして、肺内のシリカの量の多い肺線維症の方は、少ない肺線維症の方に比べて生存期間がより短くなっていることもわかりました(図3B)。
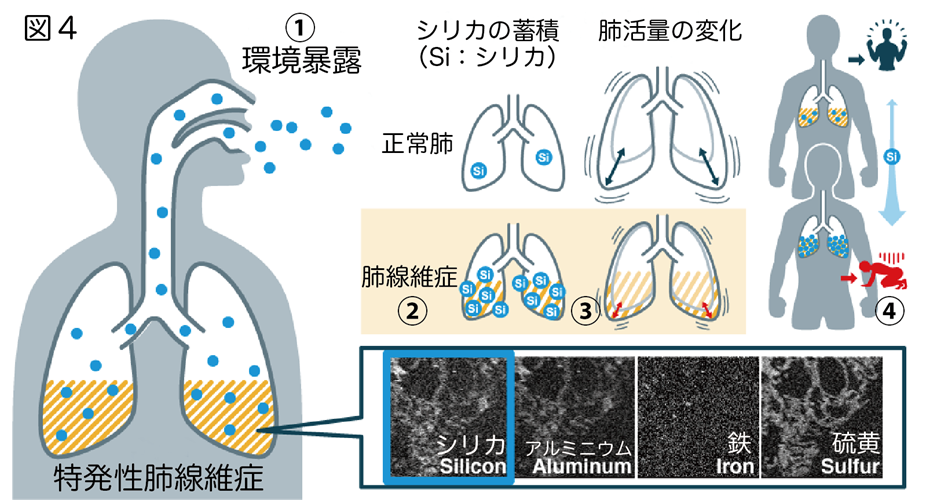
本研究結果から得られた、肺線維症における吸入シリカの関与についてまとめてみました(図4)。
肺線維症の患者さんでは、生活環境や職業性環境から吸入されるシリカ(図4(1))が肺内で異常に蓄積してしまい(図4(2))、徐々に肺が硬くなることで肺活量が早いスピードで減ってしまいます(図4(3))。その結果、肺線維症が進行して予後が不良となってしまうことが考えられました(図4(4))。
成果の意義
本研究で検出された結晶性シリカは、環境汚染物質であるPM2.5や季節性に本邦に飛来してくる黄砂の主成分であることが報告されています1-3。本研究の成果によって、このような大気中のシリカ吸入の予防医学の発展や、産業衛生上の吸入予防の取り組みが進み、肺に蓄積したシリカを除去できる様な治療薬が開発されることが期待されます。その結果として、肺線維症に苦しむ患者さんだけでなく、肺線維症の発症予防にもつながる可能性があると考えられます。
用語説明
注1)特発性肺線維症
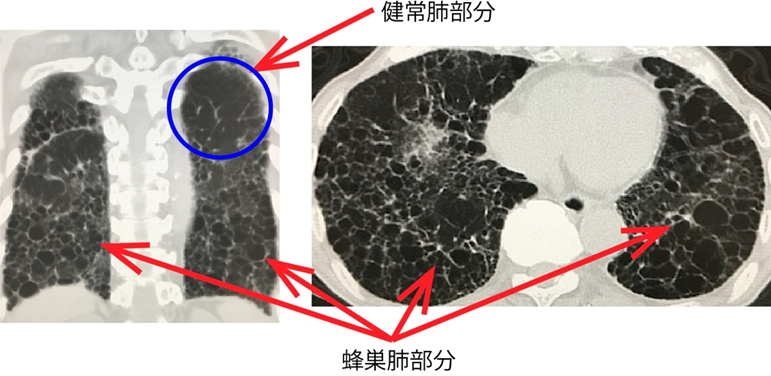
国が指定している難病疾患名は特発性間質性肺炎。特発性間質性肺炎の中でも下記のように肺の一部、特に肺底部と言われる下側の部分が蜂の巣の横断面の様に変化してくる集団が特に予後不良と言われています。そのため、このような肺の変化を蜂巣肺と呼び、蜂巣肺を来す予後不良な間質性肺炎を特別に特発性肺線維症というグループに分けています。国が難病に指定しているのは、特発性間質性肺炎の中でも、蜂巣肺の変化を起こす特発性肺線維症です。
注2)シリカ
シリカには結晶性シリカと非結晶性シリカがあり今回私たちが肺の中で検出したのは結晶性シリカです。結晶性シリカは石英の主成分であり、ケイ素とも呼ばれています。非結晶性シリカは水溶性であり人体への毒性ははっきりしていませんが、結晶性シリカは石英の採掘業務の従事などで過剰に吸入することによって珪肺症と呼ばれる塵肺症を発症することが知られています。健康被害、ならびに環境汚染物質として注目されているPM2.5, PM10の元素解析では、シリカが主成分であることが報告されており1, 2、4-5月に日本に飛来してくる黄砂もシリカが主成分(約70%)と報告されています3。2021年には肺線維症の急性増悪にPM2.5が関与しているという報告がされたばかりです6。
注3)大気マイクロ粒子線励起X線分析(In-air micro-PIXE)
In-air micro-particle induced X-ray emissionを略してin-air micro-PIXEと呼んでいます。高速に加速したイオンビームを物質に照射することで、その物質に含まれる元素固有のエネルギーのX線が放出されます。ケイ素(シリカ)、マグネシウム、アルミニウムなど全ての元素に固有のX線エネルギーがあり、X線のエネルギーと強度からイオンビームが照射された物質にどんな元素が含有されているかを分析でます。イオンビームはX線を放出させる能力が高いので、極めて微量(ppm)の元素であっても検出できるのが特徴です。
本研究は日本学術振興会の研究費を用いて行われました。
(JSPS KAKENHI) (No.20K12493)
本研究成果は、以下のタイトルと共著者らで国際環境雑誌『Environmental Science & Technology Letters』に発表されました。
Progression of idiopathic pulmonary fibrosis is associated with silica/silicate inhalation
Yasuhiko Koga1#, Takahiro Satoh2, Kyoichi Kaira3, Yoshimasa Hachisu1, Yasuyuki Ishii2, 4, Toshiki Yajima 5, Takeshi Hisada6, Hideaki Yokoo7, Kunio Dobashi8
#責任著者
1Department of Respiratory Medicine, Gunma University Graduate School of Medicine
2 Takasaki Advanced Radiation Research Institute, National Institutes for Quantum and Radiological Science and Technology
3 Department of Respiratory Medicine, International Medical Center, Saitama Medical University
4 Biological function analysis, Gunma University Graduate School of Medicine
5 Department of General Surgical Science, Gunma University Graduate School of Medicine
6Gunma University Graduate School of Health Sciences
7Department of Human Pathology, Gunma University Graduate School of Medicine
8Jobu Hospital for Respiratory Diseases
参考文献
1. Talbi, A.; Kerchich, Y.; Kerbachi, R.; Boughedaoui, M., Assessment of annual air pollution levels with PM1, PM2.5, PM10 and associated heavy metals in Algiers, Algeria. Environ Pollut 2018, 232, 252-263.
2. Xue, H.; Liu, G.; Zhang, H.; Hu, R.; Wang, X., Similarities and differences in PM10 and PM2.5 concentrations, chemical compositions and sources in Hefei City, China. Chemosphere 2019, 220, 760-765.
3. He, M.; Ichinose, T.; Song, Y.; Yoshida, Y.; Arashidani, K.; Yoshida, S.; Liu, B.; Nishikawa, M.; Takano, H.; Sun, G., Effects of two Asian sand dusts transported from the dust source regions of Inner Mongolia and northeast China on murine lung eosinophilia. Toxicol Appl Pharmacol 2013, 272, (3), 647-55.
4. Azuma, A.; Nukiwa, T.; Tsuboi, E.; Suga, M.; Abe, S.; Nakata, K.; Taguchi, Y.; Nagai, S.; Itoh, H.; Ohi, M.; Sato, A.; Kudoh, S., Double-blind, placebo-controlled trial of pirfenidone in patients with idiopathic pulmonary fibrosis. Am J Respir Crit Care Med 2005, 171, (9), 1040-7.
5. Raghu, G.; Brown, K. K.; Costabel, U.; Cottin, V.; du Bois, R. M.; Lasky, J. A.; Thomeer, M.; Utz, J. P.; Khandker, R. K.; McDermott, L.; Fatenejad, S., Treatment of idiopathic pulmonary fibrosis with etanercept: an exploratory, placebo-controlled trial. Am J Respir Crit Care Med 2008, 178, (9), 948-55.
6. Tahara, M.; Fujino, Y.; Yamasaki, K.; Oda, K.; Kido, T.; Sakamoto, N.; Kawanami, T.; Kataoka, K.; Egashira, R.; Hashisako, M.; Suzuki, Y.; Fujisawa, T.; Mukae, H.; Suda, T.; Yatera, K., Exposure to PM2.5 is a risk factor for acute exacerbation of surgically diagnosed idiopathic pulmonary fibrosis: a case-control study. Respir Res 2021, 22, (1), 80.
