概要
京都大学複合原子力科学研究所 杉山正明教授、 自然科学研究機構生命創成探究センター 加藤晃一教授(分子科学研究所/名古屋市立大学兼任)、名古屋市立大学大学院薬学研究科 矢木宏和准教授、柚木康弘同博士後期課程学生 (現:京都大学複合原子力科学研究所 研究員)、量子科学技術研究開発機構 量子生命科学研究所 河野秀俊グループリーダー、松本淳同主幹研究員、ラウエ・ランジュバン研究所(フランス)ポルカ―博士、マーテル博士らの国際共同研究グループは、中性子・X線小角散乱をはじめとした複数の実験データと計算機によるモデリングおよびシミュレーション技法を統合した解析手法で、時計タンパク質が振動周期中で形成する24個もの分子からなる巨大複合体の全長構造とダイナミクスの解析に成功し、この巨大複合体が概日リズムを制御する仕組みの一端を明らかにしました。
本研究は実験科学と計算科学の発展と統合によって、X線結晶構造解析や低温電子顕微鏡といった既存の構造生物学手法では困難であった揺らぎを含む巨大タンパク質複合体の構造を明らかにしました。この統合解析手法は同様の巨大複合体に適用することで生命科学に新たな知見をもたらすと期待されています。
本成果は、2022年3月10日に英国の国際学術誌Communications Biologyにオンライン掲載されます。

1.背景
ヒトの体温、心拍数、ホルモン分泌のような生理機能に関連する事象には24時間周期が認められます。こうした周期現象は日照時間や潮の満ち引きと同様に地球の自転周期と呼応しており、概日リズムと呼ばれて、生物時計によって制御されていることが知られています。
シアノバクテリアの生物時計はたった3種類の時計タンパク質KaiA、KaiB、KaiCで制御されており、これらは自律的に24時間周期で離散・集合を繰り返します。この離散・集合の概日リズムの発現機構を理解するためには時計タンパク質が形成する各種複合体の溶液構造を解明することが重要です。しかし、この周期の中で現れるKaiA-KaiB-KaiCによる巨大な複合体(ABC複合体)は、低温電子顕微鏡で部分構造[注1]が解かれましたが、運動性が高いと予測されるKaiAのN末端側ドメイン[注1]を含む全長構造[注1]は未解明でした。
溶液中で現れるこのABC複合体の全長構造の解明には、以下の3つの課題が存在しました。
課題1:凝集体や解離成分が共存する溶液中から、ABC複合体を選択して観測すること。
課題2:高い運動性を持つKaiAの挙動を解明するために、複合体の中からKaiAを選択して観測すること。
課題3:課題1,2を解決した上で、巨大な複合体の構造とダイナミクスの解析手法を開発すること。
本研究チームは課題の克服に取り組み、ABC複合体のダイナミクスを含む全長構造の解明を行いました。
2.研究手法・成果
本研究では課題1を解決するために、ゲルろ過クロマトグラフィー (SEC) による成分分離と連結してX線・中性子小角散乱 (SAXS・SANS) [注2]を行う最新手法である「SEC-SAXS・SEC-SANS法」を用いて、多成分溶液中のABC複合体のみの散乱プロファイルを取得しました (図1(a))。課題2を解決するために、SEC-SANS測定では重水素化ラベル試料を用いた逆転コントラストマッチング (iCM) 法 [注3]と組み合わせた「SEC-iCM-SANS法」を採用し、ABC複合体中の12個のKaiAの部分構造に由来する散乱プロファイルの取得に成功しました。更に、新たな計算解析法を構築して散乱プロファイルから溶液中でのABC複合体の構造・ダイナミクスを再現するモデルを得ることに成功しました。具体的には、先行研究で解明されていないABC複合体中のKaiAの配置を様々に変化させた2000万個の全長構造モデルを作成し、その中から上記の散乱プロファイルを再現する構造モデルを選別し、更にその選別されたモデルを初期構造として分子動力学 (MD)シミュレーション[注4]を行い、安定な構造を最適モデルとして採用しました(図1 (b))。
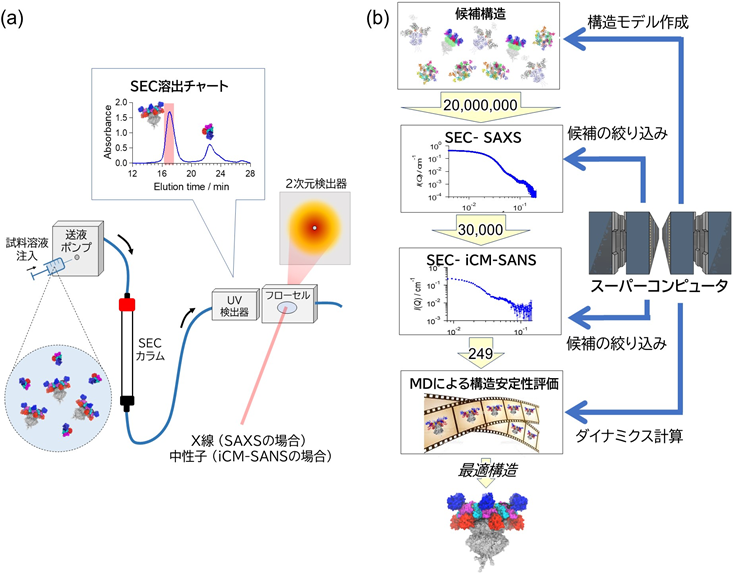
図1:(a)SEC-SAXS・SEC-iCM-SANSの模式図。SECで成分分離を行うことで特定の成分を選択測定が可能となり、複合体解析で課題となる多成分性が解消しました。
(b) 計算機を用いた解析フローチャート。可能なKaiAの配置を持つ全ての構造を作成し、SEC-SAXS・SEC-iCM-SANSを用いてスクリーニングを行い、最後にMDで構造安定性を評価して最適構造を採用しました。
本研究では上記の実験と計算科学の統合アプローチによって、ABC複合体の全長構造およびダイナミクスを明らかにすることができました。特に、これまで捉えられていなかったKaiAのN末端側の2つのドメイン(図2、赤と青)の配置とそのダイナミクスが解明されたことは大きな成果です。具体的には、図2(c)で示すように青のドメインは、複合体の最上段に位置しKaiCとの相互作用可能な界面を覆い隠すように運動しており、この位置への溶液中のKaiCの結合を阻害していることが示唆されました。本結果から、Kaiタンパク質のシステムは、ABC複合体が形成された際には、KaiAの運動によって溶液中のKaiCとの不要な相互作用を阻害することで、解離・会合からなる概日リズムを制御していることが明らかになりました。
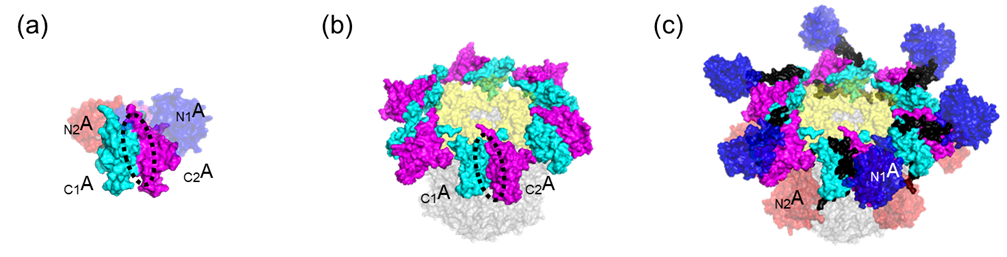
図2:ABC三者複合体上のKaiAの立体配座。KaiAは2量体であり、各単量体は2つのドメインを持っています。図では、1つのKaiAのN末端側ドメインとC末端側ドメインをそれぞれN1A(青)とC1A(水)、もう一つのKaiAのN末端側ドメインをN2A(赤)とC末端側ドメインをC2A(紫)として、色で塗り分けて表しています。
(a) KaiA2量体上のKaiCとの相互作用界面 (黒点線枠) を示しています。
(b) 低温電子顕微鏡により解かれたABC複合体の構造です。KaiA2量体のN末端側ドメインであるN1A(青)とN2A(赤)が観測されていません。そのため、(a)で示した相互作用界面が外部に暴露しています。
(c) ABC複合体の全長構造です。NAとCAをつなぐループを黒で示していますが、特に今回解明したN1Aとループの配置が、相互作用面が暴露することを防いでいる様子を捉えています。
3.波及効果、今後の予定
溶液中で運動性の大きなABC複合体中のKaiAの構造を解明することは、構造生物学において最も注目される手法である低温電子顕微鏡をもってしても困難でした。本研究では最新の中性子溶液散乱法を始めとする複数の実験手法を組み合わせることで必要な構造情報を取得し、さらに計算科学的手法と統合することによって、この困難を解決することができました。
生理環境に近い「溶液中」の構造とダイナミクスを解明することは生命現象の理解には欠かせませんが、本研究開始時に挙げられていた3つの課題は、多くの生体超分子の構造解析においても同様に見受けられます。したがって、本研究で確立した統合アプローチは、今後構造生物学の発展に大きく寄与すると期待されます。
4.研究プロジェクトについて
本研究は、京都大学複合原子力科学研究所、自然科学研究機構生命創成探究センター、同分子科学研究所、名古屋市立大学大学院薬学研究科、量子科学技術研究開発機構量子生命科学研究所、総合科学研究機構中性子科学センター、立命館大学、ラウエ・ランジュバン研究所(フランス)の国際共同研究により実施されました。また本研究は、京都大学研究連携基盤次世代研究者支援、京都大学複合原子力科学研究所所内助成金、日本学術振興会科学研究費補助金 特別研究員奨励費(JP18J21063, JP19J15602)、研究活動スタート支援 (JP20K22629)、基盤研究S(JP18H05229)、同基金 基盤研究C(JP17K07361, JP17K07816, JP18K06101, JP19KK0071, JP20K06579)、国際共同研究強化B(JP19KK0071)、若手研究(JP19K16088, JP21K15051)、文部科学省 新学術領域研究(JP18H05534)、日本医療研究開発機構創薬等ライフサイエンス研究支援基盤事業創薬等先端技術支援基盤プラットフォーム(BINDS)(JP20am0101106)等の支援を受けて行われました。
<用語解説>
[注1]
ドメイン・部分構造・全長構造:タンパク質はアミノ酸残基の連なりで形成されます。ドメインとは数十から数百個分のアミノ酸残基からなるタンパク質の構造単位で、KaiAは2つのドメインから形成されます。タンパク質中の一部のドメインの構造を部分構造、タンパク質中の全ドメインの構造を全長構造と呼びます。
[注2]
X線・中性子小角散乱(SAXS・SANS):試料溶液にX線・中性子を照射し、小角(約10°以下)での散乱強度を精密に測定します。得られた散乱強度の角度依存性(= 散乱プロファイル)から、溶液中の分子の大きさや分子の対称性といった構造情報を抽出することが可能です。
[注3]
逆転コントラストマッチング(iCM)法:中性子溶液散乱において75%重水素化されたタンパク質は100%重水溶媒中で散乱的に不可視化されることを利用しています。本研究ではKaiBとKaiCを重水素化して不可視化し、ABC複合体中のKaiAの部分構造を抽出することに成功しました。
[注4]
分子動力学 (MD) シミュレーション:着目する分子をある力場に置き、ニュートン方程式を解くことで、時間依存的な分子の動きを計算する手法です。近年スーパーコンピューターの演算処理能力の向上に伴い、ABC複合体のような巨大タンパク質複合体であっても適用が可能となりました。
<研究者のコメント>
小角散乱と計算科学を組み合わせることで立体配座が複雑で比較的大きな揺らぎを有する構造を特徴付けることが出来ます。こうしたタンパク質のダイナミクスは機能発現機構の理解に重要であり、立体配座を解き明かすだけではなく、構造生物学の発展に資する研究成果を示すことができたと考えています。(杉山正明)
<論文タイトルと著者>
タイトル:
Overall structure of fully assembled cyanobacterial KaiABC circadian clock complex by an integrated experimental-computational approach(実験と計算科学の統合アプローチにより解明されたシアノバクテリアの時計タンパク質KaiABC複合体の全長構造)
著 者:
柚木康弘1, 2 ǂ, 松本淳3 ǂ, 守島健4, Anne Martel5, Lionel Porcar5, 佐藤信浩4, 與語理那1, 2, 6,
富永大輝7, 井上倫太郎4, 矢木真穂1, 2, 6, 奥田綾4, 清水将裕4, 裏出令子4, 寺内一姫8,
河野秀俊3, *, 矢木宏和1, *, 加藤晃一1, 2, 6, *, 杉山正明4, *
1名市大院薬, 2自然科学研究機構生命創成探究センター, 3量子科学技術研究開発機構, 4京大複合研, 5Institut Laue–Langevin, 6自然科学研究機構分子科学研究所, 7総合科学研究機構中性子科学センター, 8立命館大・生命科学, ǂ共同第一著者, *共同責任著者
掲 載 誌:Communications Biology DOI:10.1038/s42003-022-03143-z
