発表のポイント
- 認知症モデルマウス1)で、細胞内のタンパク質凝集体をオートファジー2)による分解に導くタンパク質p62を欠損させると神経細胞に対する毒性が高いタウオリゴマー3)が脳に蓄積し、脳萎縮と脳内炎症4)が亢進することを発見。
- p62を介したオートファジーがタウオリゴマーを分解し、認知症で生じる神経細胞死や脳内炎症を抑制することを初めて明らかに。
- 本成果はp62とオートファジーを標的とした認知症の発症や進行を抑制する方法の開発に寄与すると期待。
概要
国立研究開発法人量子科学技術研究開発機構(理事長 平野俊夫)量子生命・医学部門 量子医科学研究所 脳機能イメージング研究部の佐原成彦グループリーダー、小野麻衣子研究員らは、オートファジー受容体タンパク質p62を介したオートファジーが、認知症の原因とされるタウタンパク質凝集体の中でも、神経細胞に対する毒性が高いタウオリゴマーを分解することで、認知症の病態を抑制することを明らかにしました。
細胞には、細胞内の不要なタンパク質やその凝集体などを選択的に分解して、恒常性を維持するしくみが備わっています。選択的オートファジーはそのしくみのひとつで、分解対象の選択にはオートファジー受容体タンパク質が介在しています。
アルツハイマー病などの認知症で、脳内に蓄積する異常なタウタンパク質も、選択的オートファジーによって分解されている可能性が報告されています。通常、神経細胞の骨格構造の安定化などに働いているタウタンパク質が、認知症では、異常にリン酸化して凝集体を形成した後、神経細胞質中で凝集体が束になって線維化して沈着する神経原線維変化5)を生じ、神経細胞死を引き起こすと考えられています。しかし、このうち、どのような過程の異常なタウタンパク質が選択的オートファジーで分解されるかなど、詳細は明らかではありませんでした。
そこで、オートファジー受容体タンパク質の中でも、神経原線維変化の中に一緒に沈着することで知られるp62に着目し、脳の神経細胞に異常なタウタンパク質が蓄積する認知症モデルマウスでp62を欠損させた時に、脳におよぼす影響を調べました。その結果、記憶に関わる海馬という領域で、タウタンパク質凝集体の中でも神経細胞に対して高い毒性を示すタウオリゴマーの蓄積が増加し、脳の萎縮と炎症が亢進することを発見しました。
これは、p62を介した選択的オートファジーが、タウオリゴマーを分解することで、脳の神経細胞死や炎症といった認知症の病態を抑制することを、生体脳で初めて示した成果です。現在、タウタンパク質の凝集の各過程に作用する認知症治療薬の開発が世界中で行われている中で、本成果は、タウタンパク質を標的とした認知症の発症や進行を抑制する方法の開発に、重要な手がかりをもたらします。
本研究成果は、老化の生物学分野でインパクトの大きい論文が数多く発表されている英国の解剖学会誌「Aging Cell」のオンライン版に2022年6月4日(土)午前8時(日本時間)に掲載されました。
研究開発の背景と目的
超高齢化が進む日本では、認知症患者数の増加が社会問題となっています。2025年には高齢者の5人に1人が認知症有病者になると推計され、認知症による社会的コストは年間10兆円を超えると推定されています。認知症の根本的な治療法は開発されていないことから、現時点では発症・進行をくい止められません。
アルツハイマー病などの認知症では、神経細胞が死ぬことで、物忘れや運動障害、精神症状などの多彩な症状が出現します。認知症の脳では、異常なタウタンパク質の凝集体が神経細胞やグリア細胞6)に蓄積することが知られています。異常なタウタンパク質凝集体は、凝集の過程で神経細胞にダメージを与え、細胞死を引き起こすと考えられています(図1)。
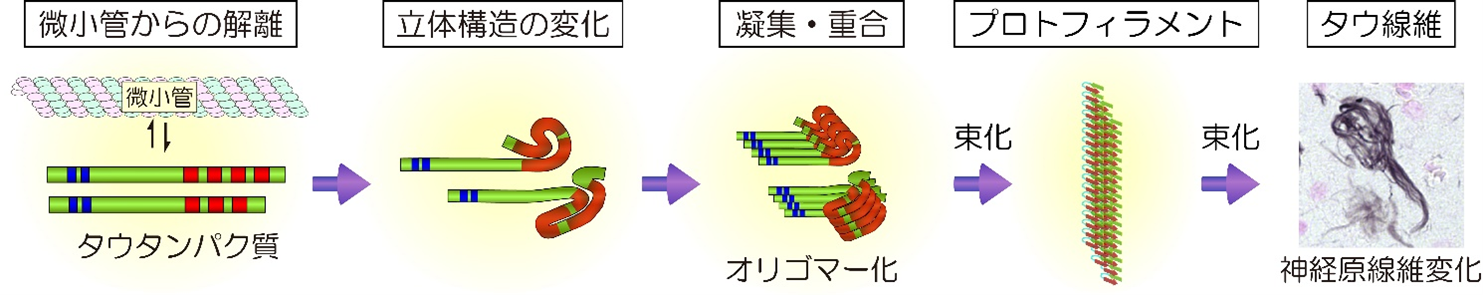
図1. 異常なタウタンパク質が凝集する過程
本来、細胞内の不要なタンパク質やその凝集体は、細胞の持つタンパク質分解機構により分解されることで、細胞の恒常性が維持されています。タンパク質分解機構のひとつであるオートファジーは、従来、こつ然と生じた膜(隔離膜)が細胞質成分を非選択的に取り込み丸ごと分解すると考えられていました。ところが、近年、ユビキチン7)というタンパク質を目印に、それが結合したタンパク質凝集体や、古くなったミトコンドリアなどを選択的に分解することがわかってきました。このしくみは選択的オートファジーと呼ばれ、オートファジー受容体タンパク質によって、選択的に分解される物質と隔離膜がつながります。
異常なタウタンパク質も、選択的オートファジーのしくみにより分解される可能性が報告されていました。一方で、どのような凝集過程の異常なタウタンパク質が選択的オートファジーで分解されるかなどの、詳細なしくみは明らかではありませんでした。
そこで本研究では、オートファジー受容体タンパク質の中でも、神経原線維変化の中に一緒に沈着することが知られているp62に着目し、脳の神経細胞に異常なタウタンパク質が蓄積する認知症モデルマウスで、p62を欠損させた時に、脳におよぼす影響を調べました。
研究の手法と成果
本研究で用いた認知症モデルマウス(PS19マウス)は、記憶に関わる海馬に加齢とともに異常なタウタンパク質が蓄積し、やがて神経細胞が死んで海馬が萎縮していきます。p62を欠損させたモデルマウスでは、欠損していないモデルマウスと比べて、リン酸化された異常なタウタンパク質の海馬への蓄積が増加することが明らかになりました(図2左)。続いて、海馬の容積を磁気共鳴画像(MRI)8)を用いて測定したところ、p62を欠損させた認知症モデルマウスでは、神経細胞死により引き起こされる海馬の萎縮が顕著に加速することがわかりました(図2中央)。また、脳内の免疫をつかさどるグリア細胞であるミクログリア9)やアストロサイト10)が海馬で活性化しており、炎症が亢進していることがわかりました(図2右)。
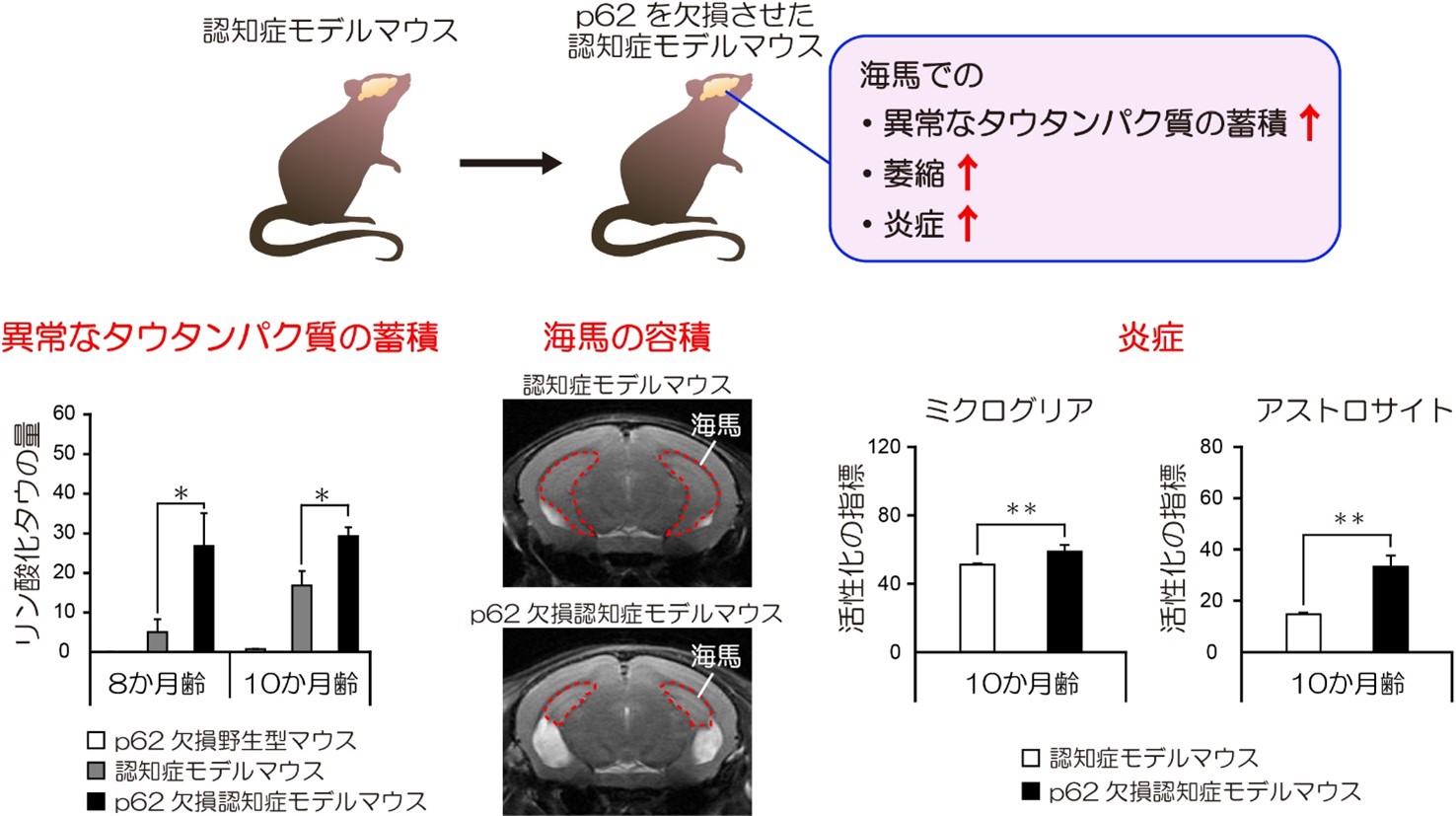
図2. p62を欠損させた認知症モデルマウス海馬の異常なタウタンパク質の蓄積、萎縮、炎症の亢進
さらに、p62を欠損させた認知症モデルマウスの海馬で蓄積が増加するタウタンパク質凝集体の種類を詳細に解析したところ、高度に線維化したタウ凝集体は増加の傾向がみられ、また、高い毒性を有すると考えられているタウオリゴマーの蓄積は顕著に増加していることがわかりました(図3)。
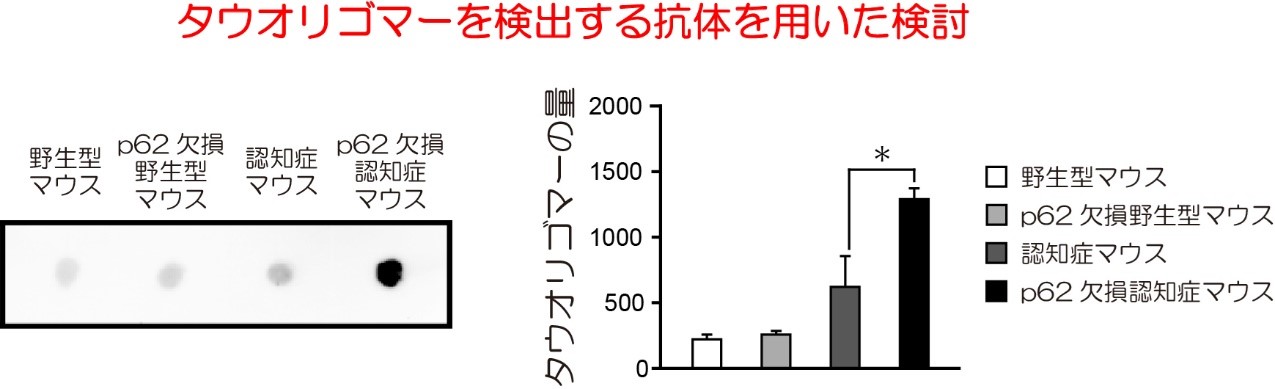
図3. p62を欠損させた認知症モデルマウスの海馬ではタウオリゴマーの蓄積が増加
我々の検証では、p62欠損野生型マウスではp62を欠損していない野生型マウスと比べて異常なタウやタウオリゴマーの顕著な蓄積は確認されていません。野生型マウスの脳では、自然に発生する異常なタウやタウオリゴマーの量が高齢でも多くないためと考えられます。
本研究では、p62タンパク質を介した選択的オートファジーのしくみが、毒性の高いタウタンパク質凝集体の蓄積を抑制する(図4)ことで、神経細胞死や炎症といった認知症の病態を抑えることを、認知症モデルマウスの生体脳で明らかとしました。
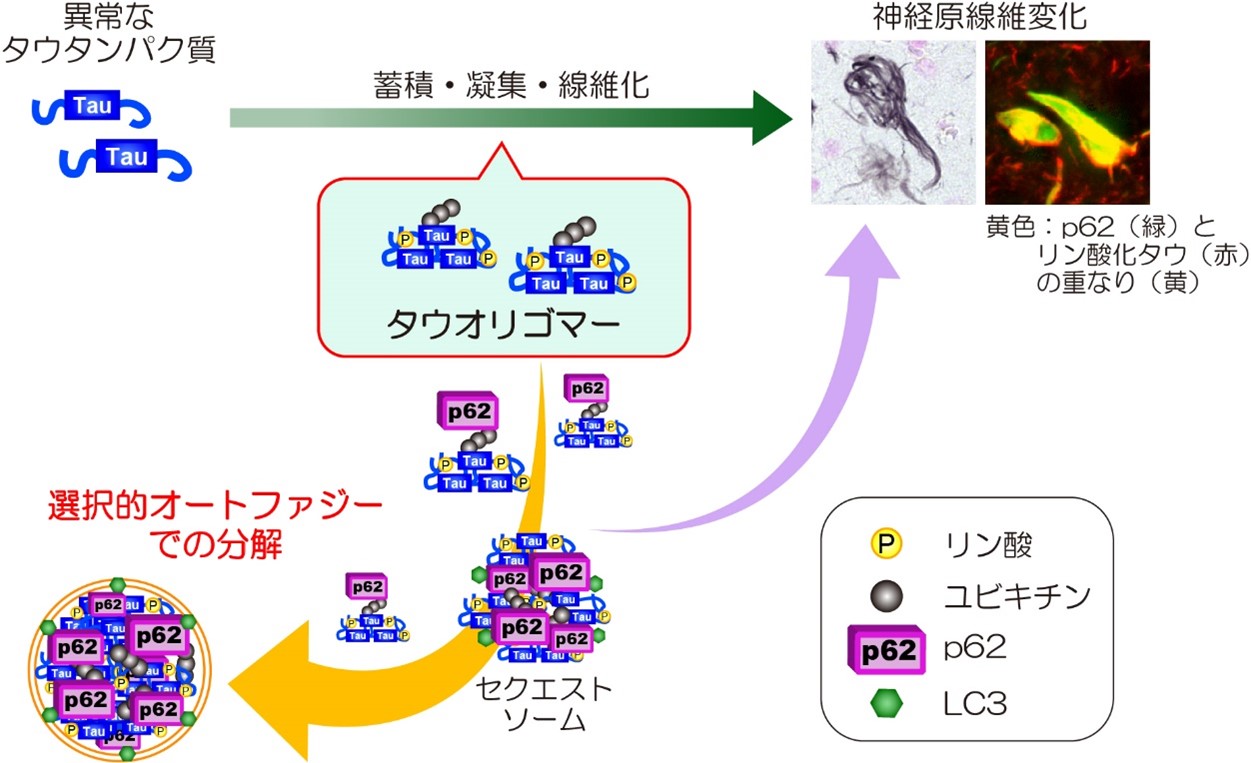
図4. p62を介した選択的オートファジーがタウオリゴマーをとりのぞくしくみ
p62は、タンパク質についた目印であるユビキチンと、オートファジーの隔離膜に含まれるLC3というタンパク質の両方に結合する性質により、ユビキチン化されたタウオリゴマーをオートファジーによる分解に導きます。p62はp62同士が結合をする性質ももっており、そのはたらきにより、ユビキチン化タンパク質をセクエストソームという膜構造を含まない顆粒状の構造体に隔離することも知られています。
オートファジー受容体タンパク質はp62以外にも存在しますが、p62は他のオートファジー受容体タンパク質と比べて特に多く脳内で発現しており(図5)、選択的オートファジーのしくみを利用して毒性の高いタウタンパク質凝集体の蓄積を抑え、認知症の発症や進行を抑制する方法を開発する上で、p62タンパク質は有望なターゲットである可能性が示されました。
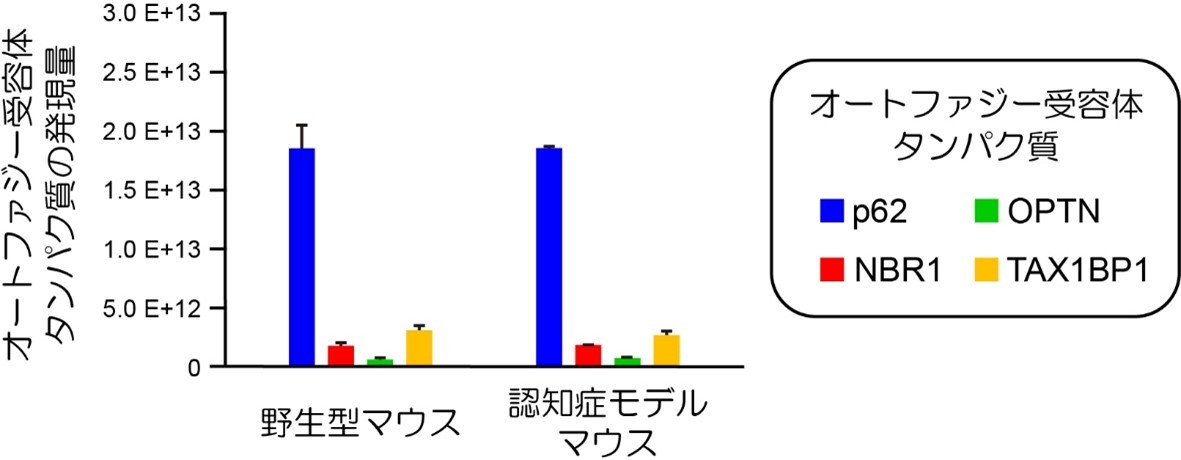
図5. マウス脳海馬のオートファジー受容体タンパク質の発現量
今後の展開
本研究で、p62タンパク質を介した選択的オートファジーのしくみが、毒性の高いタウタンパク質凝集体をとりのぞくことで認知症の病態を抑制することが、モデルマウス生体脳で明らかとなりました。これは、認知症の発症や進行を抑制する方法の開発に重要な手がかりとなります。今後、p62タンパク質や選択的オートファジーの機能を操作することによる、認知症の根本的な抑制方法の開発が期待されます。
用語解説
1)認知症モデルマウス
異常なタウタンパク質が脳内に蓄積し、加齢とともに海馬の萎縮が起きるマウス(PSマウス)。タウとは、神経細胞の骨格を形成する微小管に結合するタンパク質。アルツハイマー型認知症をはじめとする様々な精神神経疾患では、タウタンパク質が、異常にリン酸化して、凝集体を形成し、神経細胞質中で線維化して沈着することが知られています。
2)オートファジー
細胞が持つ、細胞内のタンパク質を分解するしくみのひとつ。細胞質成分を膜で取り囲み、その中身を分解する。2016年に大隅良典東工大栄誉教授がノーベル医学生理学賞を受賞したことでも有名。従来は、タンパク質を非特異的に分解するしくみと考えられてきたが、分解基質をオートファジーによる分解に導くオートファジー受容体タンパク質の働きにより、ユビキチン化されたタンパク質凝集体や細胞内小器官(オルガネラ)、細菌を選択的に分解することが近年明らかとなってきました。このしくみは、選択的オートファジーと呼ばれています。
3)タウオリゴマー
タウタンパク質が、異常にリン酸化して、凝集体を形成し、線維化していく過程において、比較的少数の異常なタウタンパク質が結合した重合体のこと。異常なタウタンパク質凝集体の中でも神経細胞に対する毒性が高いと考えられています。
4)脳内炎症
様々な要因による脳組織の傷害に伴い脳内の免疫系が活性化された状態。
5)神経原線維変化
アルツハイマー病患者脳の神経細胞にみられる病理所見で、異常にリン酸化したタウタンパク質の凝集体が、神経細胞質中で線維化して沈着した状態。
6)グリア細胞
神経系を構成する神経細胞以外の細胞の総称。
7)ユビキチン
真核生物に普遍的に見られるタンパク質の一種。他のタンパク質の修飾に用いられ、タンパク質分解、DNA修復、シグナル伝達などさまざまな生命現象に関わる。
8)磁気共鳴画像(MRI)
強力な磁場と周波数の非常に高い電磁波を用いて、身体の臓器などを色々な断面で撮影する手法。
9)ミクログリア
グリア細胞のひとつであり、脳内の免疫を担当する細胞。炎症に関連した生理活性物質の産生と放出を行うとともに、貪食能を有する。
10)アストロサイト
グリア細胞のひとつであり脳の機能と可塑性を調節する細胞。神経変性疾患のうち、進行性核上性麻痺や大脳皮質基底核変性症などは、アストロサイトに異常なタウタンパク質の凝集体が蓄積することを特徴とする。
論文について
タイトル:Central role for p62/SQSTM1 in the elimination of toxic tau species in a mouse model of tauopathy
著者:Maiko Ono1, Masaaki Komatsu2, Bin Ji1,3, Yuhei Takado1, Masafumi Shimojo1, Takeharu Minamihisamatsu1, Eiji Warabi4, Toru Yanagawa4, Gen Matsumoto5, Ichio Aoki1, Nicholas M. Kanaan6, Tetsuya Suhara1, Naruhiko Sahara1, Makoto Higuhi1
所属:
1. Quantum Life and Medical Science Directorate, National Institutes for Quantum Science and Technology, Chiba, Japan
2. Department of Physiology, Juntendo University Graduate School of Medicine, Tokyo, Japan
3. Department of Radiopharmacy and Molecular Imaging, Fudan University, Shanghai, China
4. Faculty of Medicine, University of Tsukuba, Tsukuba, Japan
5.Department of Histology and Cell Biology, Nagasaki University Graduate School of Biomedical Sciences, Nagasaki, Japan
6. Department of Translational Neuroscience, College of Human Medicine, Michigan State University, Grand Rapids, Michigan, USA
DOI: https://doi.org/10.1111/acel.13615
