お知らせ
国立研究開発法人量子科学技術研究開発機構の平野俊夫理事長が、国立大学法人北海道大学遺伝子病制御研究所の村上正晃教授と共同で、これまでの長年の研究成果を基に個人的な活動として新型コロナウイルスに関する論文を発表いたしましたので、お知らせいたします。
(以下論文概要)
論文のポイント
- 新型コロナウイルスSARS-CoV-2感染症であるCOVID-19に伴う致死的な急性呼吸器不全症候群は、免疫系の過剰な生体防御反応であるサイトカインストームが原因であると考えられる。
- サイトカインストームは、遺伝子の転写因子であるNF-kBとSTAT3の協調作用により、免疫関連タンパク質であるインターロイキン6(IL-6)の増幅回路(IL-6アンプ)が活性化され、炎症性サイトカインの産生が異常に増加し起こる。
- COVID-19にみられる急性呼吸器不全症候群の治療薬の標的としてIL-6 アンプが有望であり、IL-6-STAT3経路の阻害が有効であることを示唆した。
国立研究開発法人量子科学技術研究開発機構(以下「量研」という。)の平野俊夫理事長は、国立大学法人北海道大学遺伝子病制御研究所の村上正晃教授と共同で、新型コロナウイルス感染症(COVID-19)(1)で生じる急性呼吸器不全症候群(ARDS: Acute Respiratory Distress Syndrome)(2)がサイトカインストームにより発症するサイトカインリリース症候群(CRS: Cytokine Release Syndrome)(3)である可能性とそれを防ぐ治療標的としてIL-6-STAT3経路を提唱した。
COVID-19はパンデミック感染症となり、4月14日現在世界中の感染者は190万人、死者は12万人に達した。一刻も早くワクチンや治療薬を開発するための取組が世界中で行われている。特に重症化したCOVID-19に発症する急性呼吸器不全は致死率が高く治療方法の開発は緊急の課題である。最新の2編の論文(Zhouら、Nature 3月12日号、Hoffmannら、Cell 4月16日号)により新型コロナウイルス(SARS-CoV-2)が感染するためには細胞表面にあるアンジオテンシン変換酵素2(ACE2)(4)というタンパク質が受容体として作用することが明らかにされた。さらにHoffmannらの論文でウイルスが細胞に侵入するためには細胞表面に存在するタンパク分解酵素であるTMPRSS2が必要であることも明らかにされた。
これらの知見に基づき、これまでの本研究グループの研究成果や他の研究グループの研究成果を含めて総合的に考察した結果、転写因子であるNF-kB(5)とSTAT3(6)の協調作用により、インターロイキン6(IL-6)(7)の増幅回路(IL-6アンプ)(8)が活性化され、炎症性サイトカインの産生が異常に増加するサイトカインストームが発生することによりARDSが発症するという仕組みを提唱した。さらに治療薬の標的としてIL-6アンプで重要な役割を担うIL-6-STAT3経路が有望であることを提唱した。白血病などのCAR-T治療(9)における重篤な副作用であるCRSが抗IL-6受容体抗体で治療できる事実を踏まえ、COVID-19に見られる致死的な呼吸器不全であるARDSも抗IL-6受容体などのIL-6-STAT3経路阻害薬で治療できる可能性が高いことを示唆した。
同成果は、アメリカの免疫学雑誌Immunity 5月号に掲載予定である(4月11日からon lineで先行掲載)。
背景と目的
昨年12月に中国で発症した新型コロナウイルス感染症(COVID-19)は、パンデミック感染症となり、4月14日現在世界中の感染者は190万人、死者は12万人に達した。一刻も早くワクチンや治療薬を開発するための取組が世界中で行われている。特に急性呼吸器不全症候群(ARDS: Acute Respiratory Distress Syndrome)は致死率が高く治療方法の開発は緊急の課題である。最新の2編の論文(Zhouら、Nature 2020年3月12日号、Hoffmannら、Cell 2020年4月16日号)により、新型コロナウイルス(SARS-CoV-2)が感染するためには、サーズウイルス(SARS-CoV)と同じく細胞表面にあるアンジオテンシン転換酵素2(ACE2)というタンパク質が受容体として作用することが明らかにされた。さらにHoffmannらの論文でウイルスが細胞に侵入するためには細胞表面に存在するタンパク分解酵素であるTMPRSS2によりウイルスのスパイク蛋白が処理されることが必要であることも明らかにされた。
本研究グループは、これまでIL-6-STAT3系がどのように自己免疫疾患、炎症性疾患を誘導するか研究して、炎症誘導の基盤として「IL-6アンプ」を報告した(Ogura et al.,Immunity,29, 628-36,2008)。この機構は、気管支・肺胞上皮細胞、線維芽細胞や血管内皮細胞などの非免疫細胞に存在し、NF-kB経路とSTAT3経路の同時活性化によって種々の炎症性サイトカインやケモカイン、増殖因子などを病態局所にて大量に持続的に産生する。さらに、炎症状態では、STAT3活性化因子の主なものはIL-6であることも示唆しており、このIL-6アンプは関節リウマチなどの慢性炎症性疾患や自己免疫疾患やがんなどに関与している(Murakami et al.,Cell Rep,3,946-59,2013, Murakami et al.,Immunity,50,812-31,2019)。最近では、最先端がん治療の一つであるCAR-T細胞療法の副作用であるサイトカインストームが原因の致死性のサイトカインリリース症候群(CRS: Cytokine Release Syndrome)の治療にも抗IL-6Ra抗体などIL-6-STAT3経路の遮断が使用されている。
これらの知見に基づき、COVID-19に発症する致死的な急性呼吸器不全ARDSの発症の仕組みを考察し、その治療としてIL-6-STAT3経路遮断の有効性を示唆した。
提案の内容
ZhouらとHoffmannらは以下の点を明らかにした。1)SARS-CoV-2ウイルスの表面に存在するスパイクタンパクは、細胞表面のACE2を受容体として結合するが、細胞内に入って感染するためにはスパイクタンパクが細胞表面のタンパク分解酵素であるTMPRSS2により切断される必要がある。2)その後切断されたスパイクタンパクがウイルス膜と細胞膜の融合を引き起こす結果、ウイルスはACE2とともに細胞内に取り込まれる。3)TMPRSS2の阻害剤はウイルス感染モデル実験系においてウイルスの細胞内取り込みを阻止した。またACE2に対する抗体もウイルスの細胞内取り込みを阻止した。
したがって、SARS-CoV-2ウイルスとACE2との結合を抑制する分子や、TMPRSS2の阻害剤はウイルス感染を抑制する効果が期待され、ウイルス感染の初期には有効な治療薬になる可能性がある。また、スパイクタンパクに対する抗体、スパイクタンパク以外のウイルス膜タンパクに対する抗体やサーズウイルスや新型コロナウイルスから治癒した患者に存在する抗体なども期待される。一方、感染後期に生じる致死的な急性呼吸器不全ARDSは、ウイルスが減少し始めた頃に生じるので、過剰な生体反応であるサイトカインストームにより引き起こされるサイトカインリリース症候群CRSである。
生体にSARS-CoV-2などの外来ウイルスが感染すると自然免疫の受容体であるPattern Recognition Receptors (PRRs)と呼ばれている分子がウイルス由来核酸などで活性化され自然免疫が活性化される(10)。SARS-CoV(SARS感染症のコロナウイルスでウイルス遺伝子配列はSARS-CoV-2のそれと約80%同じである)では、主に細胞内に存在しウイルス核酸を認識するPRRsのRIG-1やMDA5が活性化されてMYD88を介して転写因子であるNF-kBが活性化される。その結果、TNFa、IL-1、IL-6やタイプ1インターフェロン産生が誘導される。TNFaやIL-6は樹状細胞、マクロファージや好中球などの自然免疫細胞を活性化する。この自然免疫活性化に引き続き獲得免疫(10)が活性化されてウイルスを排除する。新型コロナウイルスのような新規のウイルスでは、獲得免疫の免疫記憶がないのでウイルスの完全な排除には時間がかかる。基礎疾患などを含めて何らかの原因で、ウイルス排除のための免疫反応、炎症反応が過剰に激しくなると肺胞上皮細胞などの細胞死も生じて、全身性のサイトカインストームからCOVID-19に見られる致死的なARDSが起こる。
SARS-CoV-2ウイルス感染の場合、炎症誘導にはその細胞受容体であるACE2が関連する経路も活性化して炎症誘導に関連する。前述したように、SARS-CoV-2が細胞に感染すると細胞膜上のACE2発現が減少し、そのリガンドであるアンジオテンシン2(AngII) が増加し、アンジオテンシン受容体タイプ1(AT1R)との結合を介して炎症増強作用を発揮する。実際、SARS-CoVによるARDSがAT1R阻害剤で阻止できることも報告されている。
AngII-AT1R経路は血圧を上げる作用があるが、この経路は細胞膜上の蛋白質分解酵素であるADAM17を活性化し、細胞表面状の膜型TNFaやIL-6受容体a(IL-6Ra)を切断し、可溶性TNFaや可溶性IL-6Ra(sIL-6a)が放出される。TNFaはその受容体を介して、PPRsの刺激と同様に転写因子NF-kBを活性化し、IL-6など標的分子を誘導する。IL-6-sIL-6R複合体は、非免疫細胞に作用し転写因子であるSTAT3を活性化する。その結果、肺胞上皮細胞を含む非免疫細胞では、NF-kBとSTAT3の同時活性化が生じ、過剰なNF-kB刺激がIL-6増幅機構(IL-6 アンプ:IL-6 amplifier (IL-6Amp))となり炎症性病態を形成する。IL-6アンプは活性化すると自身をさらに活性化するというポジティブフィードバック機構を有しており、一旦活性化されると際限なく活性化される性質を有しており、その結果サイトカインストームが誘導されサイトカインリリース症候群CRSが発症する。
以上を図示すると以下のようになる。
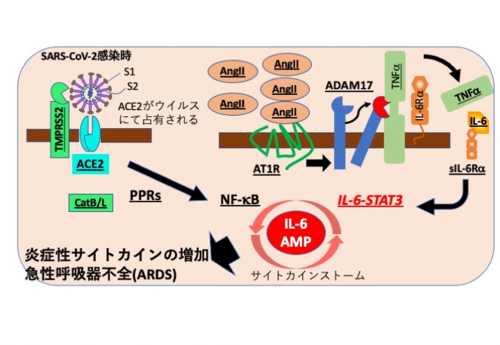
SARS-CoV-2感染時に、気管支・肺胞上皮細胞でのIL-6アンプが活性化し、その後の過剰なサイトカイン産生と急性呼吸器不全症候群(ARDS)を誘導する模式図
気管支・気道上皮細胞にてACE2に結合したSARS-CoV-2ウイルスは、TMPRSS2の作用により細胞内に取り込まれる。その後、ウイルス分子の構造を認識した細胞のパターン認識受容体(PPRs)が活性化し、下流のNF-kB経路が活性化する。さらに、感染に伴って本来ACE2に結合して分解されるアンジオテンシン(AngII)が血中に増加し、アンジオテンシン受容体1(AT1R)からの信号が過剰となる。活性化されたAT1R信号は、蛋白質分解酵素であるADAM17を活性化し、細胞膜型のTNFa、IL-6Ra、増殖因子などの炎症関連分子を可溶性のものに変換する。可溶性のTNFa、IL-6-可溶性IL-6Ra(sIL-6Ra)は、気管支・肺胞上皮細胞、血管内皮細胞を含む非免疫系細胞にてNF-kBとSTAT3を同時に活性化し、過剰なNF-kB活性化機構であるIL-6アンプを活性化、これらの細胞の局所にて過剰なサイトカインが産生される。その結果、サイトカインリリース症候群CRSが引き起こされ、COVID-19にみられる致死的な急性呼吸器不全症候群ARDSが発症すると考えられる
今後の展開
COVID-19に生じる致死的な急性呼吸器不全ARDSはサイトカインリリース症候群CRSであり、CRSを治療することができれば新型コロナウイルス感染症、COVID-19も恐ろしい病気ではなくなる。治療薬開発の有望な標的としてTMPRSS2、ACE2、AT1R、ADAM17、TNFaそしてIL-6アンプで重要な役割を果たしているIL-6-STAT3経路などが考えられる。特に、感染後期に見られる致死的なARDSの治療には、すでにCAR-T治療におけるCRSの治療に使用されており、かつIL-6アンプを阻害できる抗IL-6受容体抗体も有望である。
用語解説
1.COVID-19 … Coronavirus disease 2019、2019年新型コロナウイルス感染症。
2.急性呼吸器不全症候群 (ARDS: Acute Respiratory Distress Syndrome) … ウイルスや細菌感染による肺炎や誤嚥性肺炎、あるいは外傷や人工呼吸器などによるメカニカル損傷などにより生じる重篤な呼吸器不全に至る。
3.サイトカインリリース症候群(CRS: Cytokine Release Syndrome) … 炎症性病態誘導にてIL-6、TNFaなどの炎症性サイトカインが過剰に産生される状態をサイトカインストームという。その結果、臓器機能が不全となる症候群をサイトカインリリース症候群(Cytokine Release Syndrome)という。
4.アンジオテンシン変換酵素2(Angiotensin Converting Enzyme 2: ACE2) … アンジオテンシII(AngII)を切断するペプチダーゼで血液中のAngIIを減少させる。AngIIはその受容体であるアンジオテンシン受容体タイプ1(AT1R)を介して血圧をあげる作用がある。
5.NF-kB … 炎症反応で中心的な役割を果たす転写因子。NF-kBの活性化でIL-6、ケモカイン、増殖因子が発現される。NF-kBの活性化を誘導する因子としてはTNFa、IL-1、TLRなどがあるが病気を引き起こすような過剰な活性化は、NF-kB活性化と同時にIL-6-STAT3経路の活性化が必要である。
6.STAT3 … Signal Transducer and Activator of Transcription 3。STAT3は転写因子であり核内で機能する。サイトカイン受容体を含む信号伝達系にて活性化、細胞質から核内に移動して染色体遺伝子に結合して標的遺伝子の転写を制御する。炎症時のSTAT3活性化因子は、IL-6であり、後述するIL-6アンプ活性化時には核内でNF-kBと会合してNF-kBの活性を増強する(Ogura et al.,Immunity,29, 628-36,2008)。
7.インターロイキン6(IL-6: Interleukin 6))… インターロイキン6は、免疫反応、急性期反応、造血反応、再生、初期発生や内分泌系など生体の恒常性維持に重要なサイトカインで1986年に発見された(Hirano et al., Nature,324,73-6,1986)。また、IL-6はIL-1やTNFaとともに代表的な炎症性サイトカインで、慢性炎症性疾患、自己免疫疾患、がんの発生や悪性化、さらに老化や肥満などに伴う疾患に関与している(Hirano,Int.Rew. Immunol,16,249-84,1998, Murakami et al.,Immunity,50,812-31,2019)。
8.IL-6アンプ (IL-6 Amp: Interleukin 6 Amplifier) … 例えばサイトカイン刺激などによって、線維芽細胞や血管内皮細胞などで、転写因子であるNF-kBとSTAT3が同時に活性化すると、炎症細胞を引き寄せる因子である遊走因子ケモカインの産生が相乗的に起こる。この多量のケモカイン産生によっていろいろな免疫細胞が局所に集積して、その場の恒常性を破綻、局所炎症が誘導される(Ogura et al., Immunity, 2008)。IL-6アンプが慢性的に活性化すればいろいろな病気に関連する慢性炎症へと発展する。すでに1000遺伝子以上のIL-6アンプの正の制御遺伝子を同定し、それらには非常に高い割合にてメタボリック症候群、神経変性疾患を含む慢性炎症性疾患の関連遺伝子が存在することを見いだしている(Murakami et al.,Cell Rep,3,946-59,2013)。
9.CAR-T治療 … 患者から採取した免疫細胞であるT細胞に遺伝子改変を行い、がん細胞の目印を認識するアンテナ(キメラ抗原受容体:Chimeric Antigen Receptor、CAR)を人工的にくっつけたうえで増やし、再び体内に戻すことで、標的になるがん細胞への攻撃力を強化する治療法。2019年3月に国内で承認。
10.自然免疫と獲得免疫 … 新型コロナウイルスSARS-CoV-2のような外来抗原が体内に侵入するとはじめに反応するのが自然免疫である。樹状細胞、マクロファージ、好中球などは外来抗原を貪食して、外来抗原特異的な構造体のパターンを細胞表面、細胞内のPPRsにて認識して活性化し、ウイルス粒子やウイルス感染細胞を除去する。しかし、自然免疫系のみでは外来抗原を完全に除去することはできない。獲得免疫系が重要である。獲得免疫系は抗原特異的な免疫反応で2種類のリンパ球、B細胞とT細胞にて担われている。獲得免疫系の認識は非常に詳細なもので、遺伝子レベルで80%相同のSARS-CoV とSARS-CoV-2ウイルスを見分けることができる。B細胞は、B細胞受容体(膜型の抗体)にてウイルス粒子を直接認識して活性化、可溶性の抗体を作りウイルス粒子や感染細胞を除去する。T細胞は樹状細胞に抗原提示されたウイルス抗原をT細胞受容体にて認識し、活性化する。活性化したヘルパーT細胞は大量のサイトカインを産生してB細胞がウイルスに有効な高親和性の抗体を作成することやウイルス感染細胞を除去するキラーT細胞の免疫記憶に必須である。感染症に対するワクチンは、記憶型の獲得免疫細胞を人為的に作成することに他ならない。言い換えると自然免疫は家の1階で獲得免疫は2階のようなものである。自然免疫は獲得免疫の誘導のために必須であり、獲得免疫は自然免疫に影響する。
