 2026年3月11日
2026年3月11日
国立研究開発法人量子科学技術研究開発機構(QST)
ポイント
-
悪性黒色腫など多くのがん種で検出され、がん細胞の表面に存在する代謝型グルタミン酸1型受容体(mGluR1)1)を標的に、核種の置き換えにより同じ薬で診断と治療を行えるPET2)薬剤とα線3)標的アイソトープ治療薬4)を開発しました。
-
悪性黒色腫モデルマウスで評価を行い、PET薬剤は診断薬に必要な性質を有し、治療薬は1回の投与で原発巣のみならず、転移巣においても顕著な腫瘍抑制効果が見られ、生存期間も約2倍に延長することを確認しました。
-
本薬剤は、mGluR1の発現に基づく診断と治療の一体化を可能とするセラノスティクス薬剤として強力かつ安全な個別化医療の実現につながることが期待されます。
概要
量子科学技術研究開発機構(理事長 小安重夫、以下「QST」)量子医科学研究所 先進核医学基盤研究部の張 明栄 部長、謝 琳 主幹研究員らは、がん細胞の表面に存在する代謝型グルタミン酸1型受容体(mGluR1)を標的とするセラノスティクス薬剤の開発に成功しました。
セラノスティクスは、治療(Therapy)と診断(Diagnosis)を一体化した新しい医療技術です。放射性同位元素を用いるセラノスティクスでは、がん細胞表面に存在する分子を目印に集まる抗体や薬剤(分子標的薬)に、γ線核種やPET核種を結合させた診断薬を用いて画像検査を行い、がんの状態や薬の集積量を確認します。その後、薬に結合させる核種をα線核種やβ線核種に置き換えて治療を行います。治療前に効果の有無を予測できるだけでなく、α線やβ線が物理的に強力にがん細胞を殺傷するため、分子標的薬だけの治療や、抗がん剤、免疫チェックポイント阻害薬と比べて極めて少量の投与で治療できることから、副作用が生じにくいといったメリットがあります。
mGluR1は多くのがん種で高発現していることから、これを標的とした様々な治療薬候補が開発されていますが、セラノスティクスを可能にする診断薬と治療薬のペアはありませんでした。そこで本研究では、これまでにQSTが開発したmGluR1を標的としたα線標的アイソトープ治療薬(211At-AITM)を改良し、PET薬剤11C-IMTMとα線標的アイソトープ治療薬211At-AMTMのペアを開発しました。
悪性黒色腫モデルマウスを用いて両薬剤を評価した結果、どちらもmGluR1に強く結合しました。PET薬剤11C-IMTMは腫瘍に高集積する一方、安全性に関わる血液中や脳への集積は低く、診断薬に必要な性質を有していることを確認できました。また、α線標的アイソトープ治療薬211At-AMTMの単回投与により、皮下にがん細胞を移植して生じた原発巣だけでなく、がん細胞の血中投与により肺に生じた転移においても顕著に腫瘍増殖が抑制され、生存期間が約2倍に延長されました。
本研究によりmGluR1を標的とした初めてのセラノスティクス薬剤が開発されました。本成果は、乳がんや膵臓がん、肺がんなど幅広いがんに対して、mGluR1の発現に基づく強力かつ安全な個別化医療の実現につながることが期待されます。
本研究は、分子・細胞治療法に関する論文が数多く発表されている国際的医学誌「Molecular Therapy」に令和8年3月11日(水)(日本時間)にオンライン掲載される予定です。
研究開発の背景と目的
がんは、遺伝子に生じた変異が原因で生じます。同じ臓器のがんでも、患者ごとに変異している遺伝子が異なるため、一人ひとりの遺伝子を解析し、その変異に応じた治療を行う個別化医療が進展しています。
個別化医療において、従来の細胞障害性抗がん剤に代わる治療として、がん細胞に存在する特定の分子を狙ってその働きを制御することでがんを攻撃する分子標的治療や、免疫細胞に存在する特定の分子を狙って免疫の働きを調整し、免疫細胞によるがん攻撃を促進する免疫チェックポイント治療があります。これらの治療は、標的となる分子の有無やその量を調べて行われますが、効果を予測することは難しく、副作用の発生を予測することも難しいといった課題があります。
近年注目されているセラノスティクスは、治療(Therapy)と診断(Diagnosis)を一体化した新しい医療技術で、これを核医学分野に応用したものがラジオセラノスティクスです。ラジオセラノスティクスでは、がん細胞表面に存在する分子に集まる抗体や薬剤(分子標的薬)に、γ線核種やPET核種を結合させた診断薬を用いて画像検査を行います。その後、薬剤に結合させる核種をα線核種やβ線核種に置き換えて治療を行います。
画像検査で、がんの状態や薬の集積量を確認できるため、治療前に効果の有無を予測できます。また、α線やβ線が強力なエネルギーでがん細胞のDNAを損傷し、がん細胞を殺傷します。このため、分子標的薬だけの治療や、抗がん剤、免疫チェックポイント阻害薬と比べて極めて少量の投与で治療できることから、副作用が生じにくいといった特長があります。こうした特長からラジオセラノスティクスは、がんの個別化医療を実現する技術として期待されています。
そこで本研究では、多くのがん種で高発現しているmGluR1を標的にしたセラノスティクスを可能にするPET診断薬と標的アイソトープ治療薬のペアを開発することを目的としました。mGluR1を標的とした分子標的薬の開発は主に米国で進められていますが、第II相臨床試験5)で留まっています。これは、薬剤の性質から腫瘍の増殖抑制が持続せず効果が限定的であること、治療前の診断や、長期間の投与に伴う副作用といった課題があるためです。mGluR1を標的とするラジオセラノスティクスは、こうした課題を解決できると考えられます。
研究の手法と成果
過去にQSTで開発したmGluR1に結合する標的アイソトープ治療薬211At-AITMの化学構造を改良することにより、PET診断薬11C-IMTMとα線標的アイソトープ治療薬211At-AMTMのペアを開発しました。mGluR1を高発現しているがん種の一つである、悪性黒色腫のマウス由来細胞を用いて両薬剤の結合性を評価し、どちらもmGluR1に選択的に結合することを確認しました(図1)。
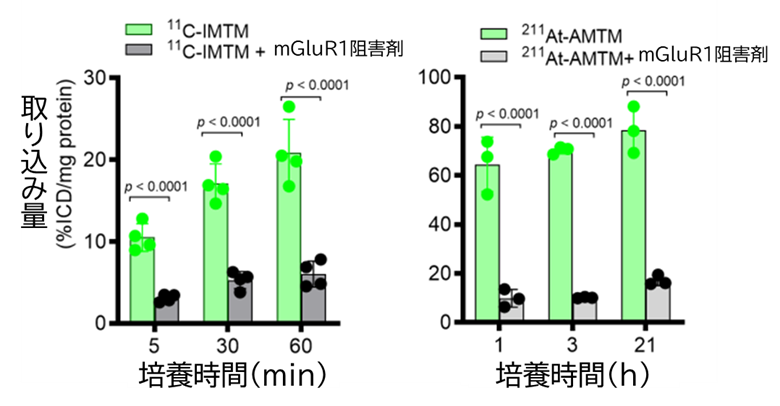
図1 マウス由来悪性黒色腫の培養細胞を用いた11C-IMTMと211At-AMTMの結合性評価
mGluR1阻害薬を添加した場合に結合性が有意に低下していることから、どちらの薬剤もmGluR1に特異的に結合していることが確認できました。
11C-IMTMのPET診断薬としての性質を評価するため、マウス由来悪性黒色腫を皮下に移植したマウスモデルに投与してPET撮像を行いました。薬剤は腫瘍部位に高集積し、集積量の定量が可能であることが確認できました(図2)。また、生体への毒性に関わる脳や血液への集積は低く、安全性も担保できていることも確認できました(図3)。
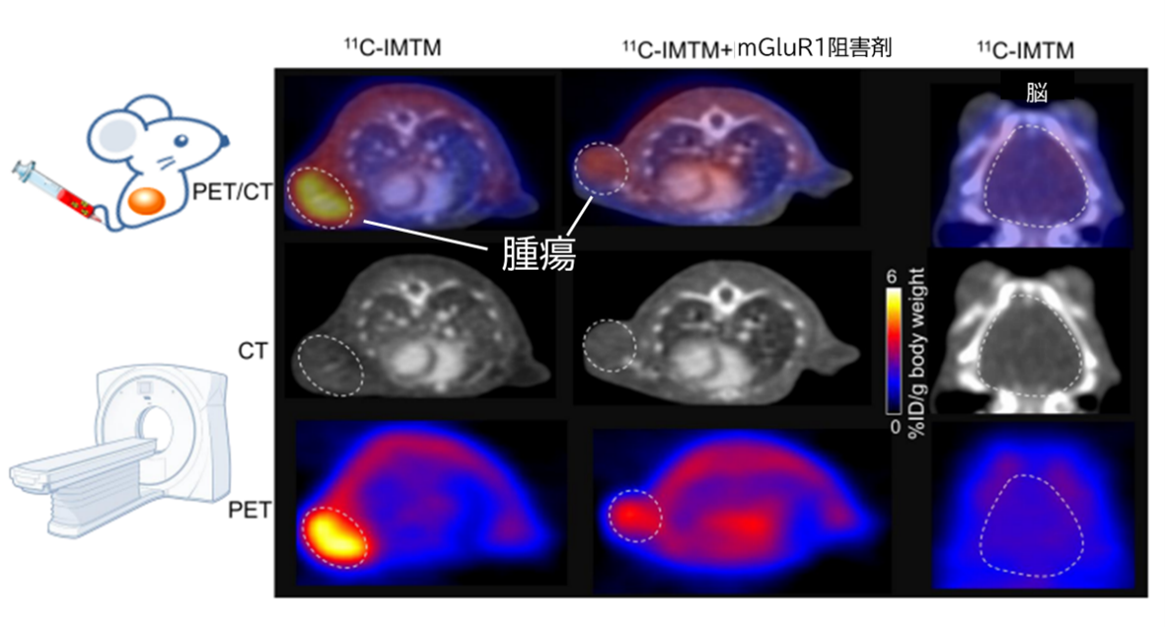
図2 悪性黒色腫マウスモデルに11C-IMTMを投与して撮像したPET画像
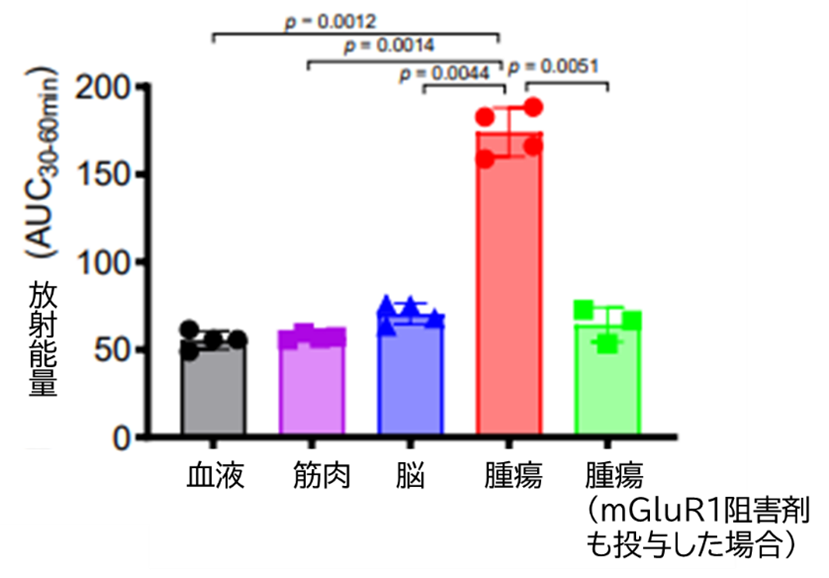
図3 各部位における11C-IMTMの放射能量
マウス由来悪性黒色腫を皮下に移植したマウスモデルに211At-AMTMを投与して治療効果を評価しました。その結果、211At-AMTMの単回投与により、全個体で腫瘍の増殖が抑制され、その効果は 10 日間持続していました(図4)。安全性の面では、血小板の一時的な減少が見られましたが、肝臓や腎臓への明らかな毒性は認められませんでした。
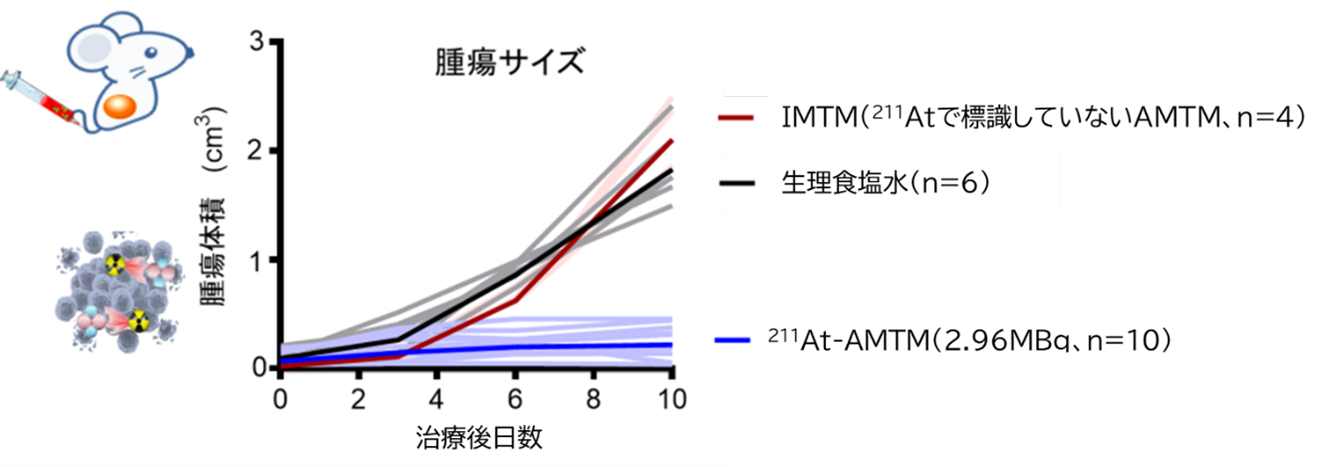
図4 悪性黒色腫皮下移植マウスモデルに対する211At-AMTM投与による抗腫瘍効果
α線標的アイソトープ治療薬は、原発巣だけでなく転移に対する治療としても期待されています。そこで、マウス由来悪性黒色腫細胞を尾静脈から投与して肺転移マウスモデルを作成し、これに対する11C-IMTMと211At-AMTMのペアによるセラノスティクスを評価しました。その結果、11C-IMTMを用いたPET撮像により肺転移巣が明瞭に可視化されました。また治療効果の面では、211At-AMTMの単回投与により生存期間が約2倍に延長されました(図5)
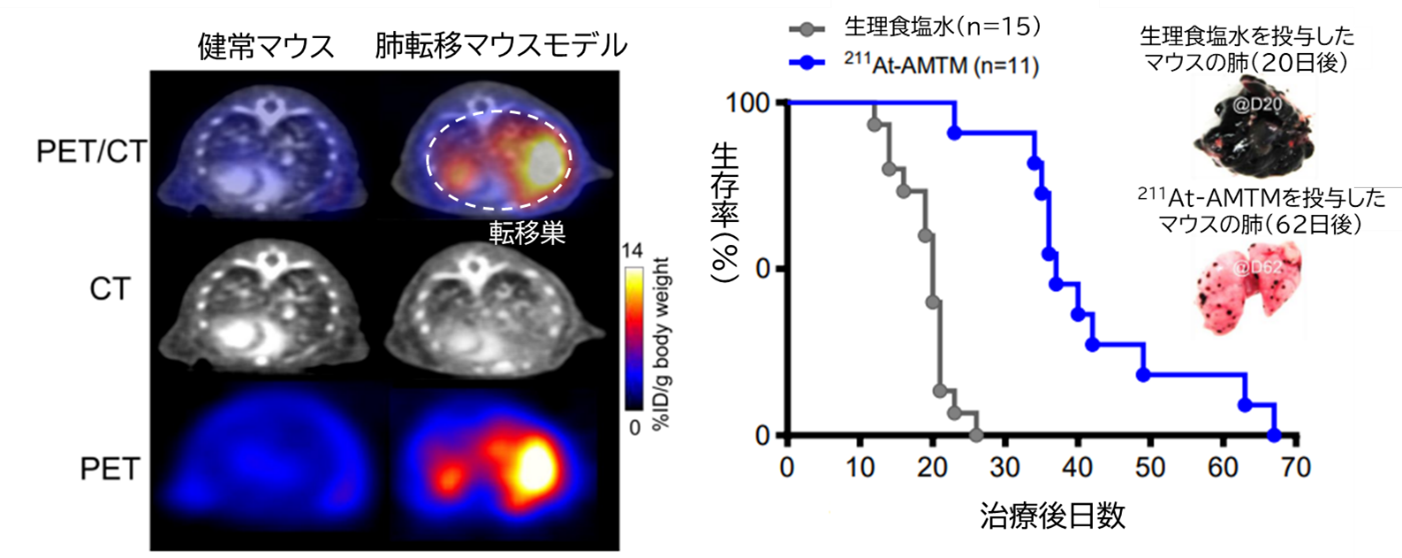
図5 肺転移マウスモデルにおける11C-IMTMと211At-AMTMのペアによるセラノスティクス評価
mGluR1が高発現しているがん種の中でも、悪性黒色腫と並ぶ難治がんである膵臓がんに対する211At-AMTMを評価しました。ヒト由来膵臓がん細胞を皮下に移植したマウスモデルに211At-AMTMを単回投与した結果、顕著な腫瘍増殖抑制効果が示され、15匹中7匹において腫瘍が消失しました(図6)。
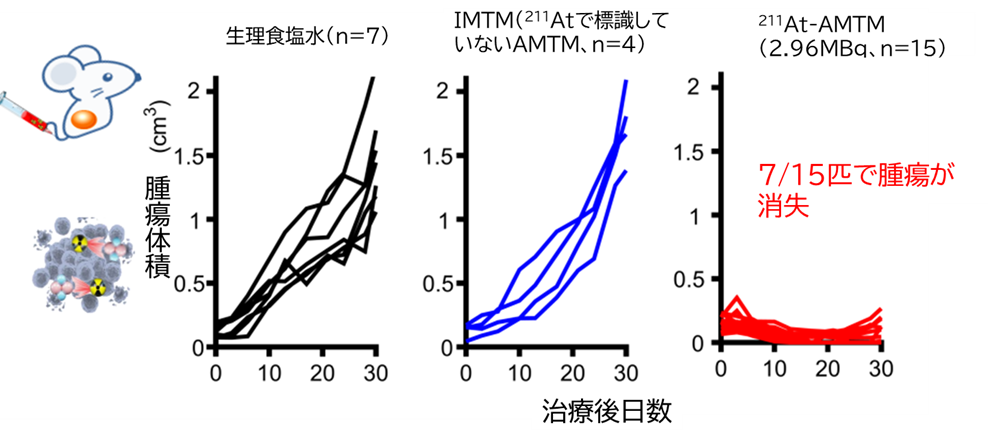
図6 膵臓がん皮下移植マウスモデルに対する211At-AMTM投与による抗腫瘍効果
今後の展開
本研究によりmGluR1を標的とした初のセラノスティクス薬剤が開発されました。本成果は、乳がんや膵臓がん、肺がんなど幅広いがんに対して、mGluR1の発現の有無や量から、がんの状態を「診て」、mGluR1を目印にがんを狙って「治す」強力かつ安全な個別化医療の実現につながることが期待されます。First-in-human試験の実施を目指して、薬剤の構造をさらに最適化し体内動態の改善と安全性や、最適な投与量、回数などの検討を進めていきます。
謝辞
本研究は、日本医療研究開発機構(AMED)「ムーンショット型研究開発事業『炎症誘発細胞除去による 100歳を目指した健康寿命延伸医療の実現』」、JSPS科研費(23H02867、24K21295、25K02613) 、武田科学振興財団「2024年度 医学系研究助成(がん領域(基礎)」の助成を一部受けています。
用語解説
1)代謝型グルタミン酸1型受容体(mGluR1)
mGluR1は中枢神経系の細胞に広く発現しているタンパク質で、記憶や学習、様々な感覚情報処理を調節しています。正常な末梢臓器では、胃に少量発現していますが、その他の臓器や組織にはほとんど発現していません。一方で、悪性黒色腫、乳がん、大腸がんなど多くの種類のがんで高い発現をしており、米国のThe Cancer Genome Atlas (TCGA)データベース6)に公開された32種類のがん(合計臨床検体数:10,967)に対して、mGluR1遺伝子の発現頻度を解析した結果、27.03% ~ 100%とばらつきはあるものの、全てのがん種において、mGluR1の発現が見られました(表1)。mGluR1は、がん細胞の増殖、転移などに関与していることがわかっており、がんの診断・治療法の開発にとって有望な標的として注目されています。
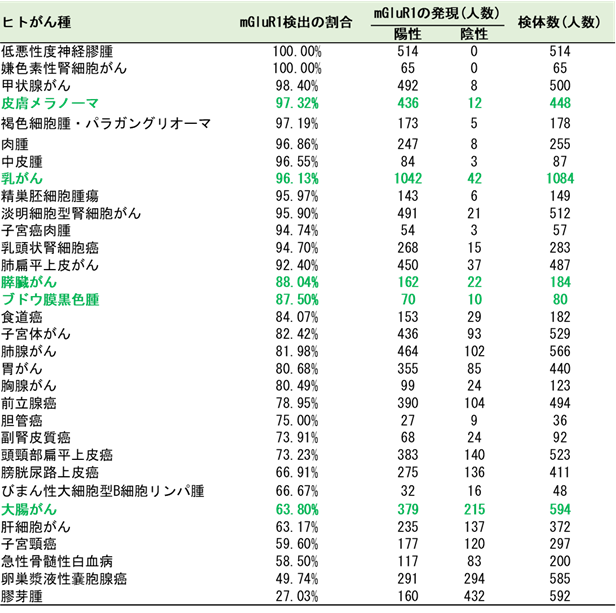
表1. 32種類のがん患者における腫瘍中のmGluR1の検出頻度
2)PET
Positron Emission Tomography(陽電子断層撮影)の略。頭文字をとり、PET 検査とも言います。身体の中の生体分子の動きをそのままの状態で外から見ることができる画像診断法の一種。18F(半減期約 2 時間)などの陽電子放出核種で標識した PET 薬剤を検査対象者に投与し、PET 薬剤より放射される陽電子に起因するγ線を検出することによって、体深部に存在する生体内物質の分布や量などを画像化します。
3) α線
α線はヘリウム(He)原子核が非常に速いスピードで飛んでいるものです。物質中を通過する際、物質と相互作用し、例えば物質中の分子が持っている電子を弾き飛ばしたり(電離といいます)することで、物質に対してエネルギーを付与します。α線は質量が大きく、物質中の分子などと衝突しやすいため、透過性が非常に低く、紙一枚で遮断することができる代わりに、物質中では短い通過距離で高いエネルギーを付与することから、分子などを密に電離することができます。α線を細胞に照射した場合、DNAに修復することが難しいキズ(DNA二重鎖切断)ができます。この現象はα線が、がん細胞を効果的に殺滅できる理由のひとつです。
4) 標的アイソトープ治療薬
細胞障害能力を有する粒子線(α線やβ線)や、光子線(γ線)を放出する放射性同位体を用いた治療法。RI内用療法、核医学治療とも呼ばれます。放射性同位体を体内に注射し、がん細胞だけを標的として、がん細胞に粒子放射線を体内から照射し殺傷します。
5) 第II相臨床試験
新しい治療法の有効性と安全性、適切な用法・用量を評価するために、比較的少人数の患者を対象として実施される段階の臨床試験です。社会実装の最終段階となる第III相試験の設計を検討するための重要なステップと位置付けられています。
【掲載論文】
タイトル:A mGluR1-targeted radiotheranostic strategy visualizes lesions and potentiates antitumor efficacy in melanoma and pancreatic cancer
著者:Lin Xie 1 , Masayuki Hanyu 1 , Masayuki Fujinaga 1 , Yiding Zhang 1 , Tomomi Kokufuta 1 , Katsushi Kumata 1 , Wakana Mori 1 , Kazui Nakamoto 1 , Takayuki Ohkubo 1 , Hidekatsu Wakizaka 1 , Katsuyuki Minegishi 1 , Lulu Zhang 1,2 ,Rui Luo 1,2 , Feng Wang 2 , Nobuki Nengaki 1 , Kotaro Nagatsu 1 , and Ming-Rong Zhang 1
著者所属:
1. Department of Advanced Nuclear Medicine Sciences, Institute for Quantum Medical Science,
2. Department of Nuclear Medicine, Nanjing First Hospital, Nanjing Medical University,
雑誌名:Molecular Therapy
