認知症モデルマウスでミクログリアが早期に活性化することを証明
さらに免疫抑制剤で神経細胞死を抑えることに成功
アルツハイマーなどの認知症の診断・治療に大きな貢献が期待される
概要
独立行政法人放射線医学総合研究所(米倉義晴理事長)分子イメージング研究センター分子神経イメージング研究グループ(須原哲也グループリーダー)の樋口真人チームリーダーは、米国ペンシルバニア大学 Virginia Lee教授・John Trojanowski教授、独立行政法人 国立病院機構 千葉東病院神経内科 吉山容正医長、独立行政法人理化学研究所脳科学総合研究センター神経蛋白制御研究チーム 西道隆臣チームリーダーらとの共同研究により、認知症のモデルマウス*1でミクログリア*2と呼ばれる細胞の活性化が脳内で早期に発生することを、PET*3用の放射性トレーサー薬剤*4による画像解析で定量的に証明することに成功しました。また、この細胞の活性化を既存の免疫抑制剤で抑えることによって、神経細胞死を防ぐことができることが明らかになりました。
同研究は、放射線医学総合研究所等が開発したトレーサー薬剤を用いた神経疾患の国際共同研究による成果であり、老人医療の分野で世界的なテーマであるアルツハイマー病をはじめとする認知症の診断や治療法の開発研究に大きな貢献が期待されます。本成果は、雑誌「Neuron」2007年2月1日号に掲載されます。
研究の背景と目的
認知症は、全世界的に極めて多数の患者数が報告されていることに加え、今後も発症数の急増が予測される難治性の神経疾患です。特に、認知症の中で50~75%を占めるアルツハイマー病の早期発見と根本治療は、老年医学分野の重要な研究テーマとして国際的に取り組まれています。高齢化が進む我が国においても、認知症の克服は、社会的な課題となっています。こうした中、放医研はPETやMRIをはじめとする豊富な画像診断技術の蓄積をもとに、2005年11月分子イメージング研究センターを立ち上げ、精神・神経疾患についても先進的な研究・開発に注力しています。最近では、放射線医学総合研究所が、大正製薬株式会社及び日本農薬株式会社と共同所有するアルツハイマー病などの神経疾患を診断するためのイメージング技術を、バイエルグループの一員である製薬会社、バイエル・シエーリング・ファーマ社(ドイツ)に供与するライセンス契約の締結を発表(2007年1月19日既報)するなど、国内のみならず世界的な医療水準の向上に寄与しています。
今回、樋口らは、米国ペンシルバニア大学の研究者であった吉山容正医師(現国立千葉東病院神経内科医長)らによって作成された認知症モデルマウスを用い、同医師らと共同して疾患の発症機構解明と診断・治療法の研究開発に取り組んできました。
研究手法と結果
(1)認知症の原因物質の1つであるタウ蛋白*5が脳内に蓄積したモデルマウスにおいては、加齢に伴って脳の海馬等において神経細胞の死滅が起こり、組織の萎縮が生じることが確認されました。
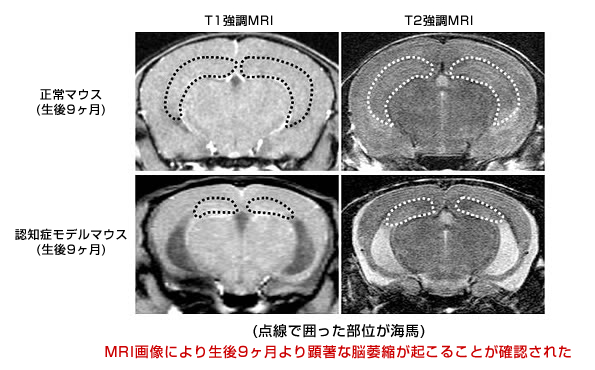
図版1 (加齢に伴う海馬の委縮)
(2)認知症モデルマウスの脳を、放射線医学総合研究所等が開発したPET用放射性トレーサーDAA1106*6を用いて画像化したところ、大脳皮質・海馬において委縮が認められる以前の段階でトレーサーの結合増加が認められ、ミクログリアの活性化が早期に起こることを定量的に実証できました。
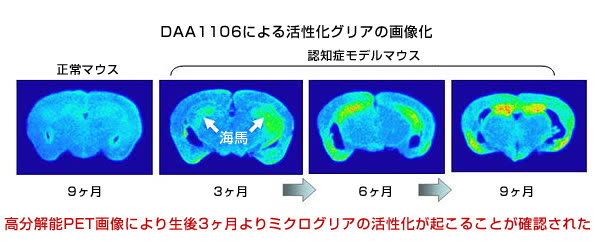
図版2 (活性化ミクログリアトレーサーの結合増加)
(3)マウスに既存の免疫抑制剤FK506を投与して、ミクログリアの活性化を抑えたところ、タウ蛋白の蓄積や海馬の萎縮が抑えられることが確認されました。
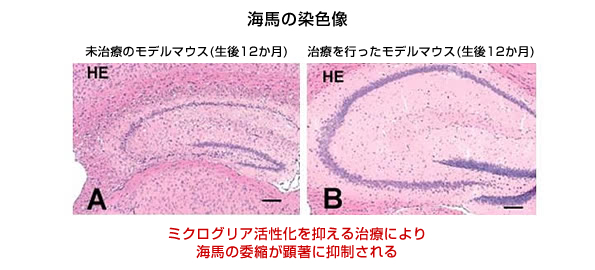
図版3 (免疫抑制剤の効果)
本研究の成果と今後の展望
モデルマウスとPET用放射性トレーサーにより、ミクログリアの活性化が認知症病理形成の早期に起こることを定量的に証明できたのは、世界初の成果です。同トレーサーは放射線医学総合研究所ですでにヒトPET検査への応用がはじまっていることから、本研究は今後、認知症の診断薬開発に大いに貢献すると考えられます。また、ミクログリアの活性化を抑えることで神経変性が抑制されることを確認できたため、認知症の治療薬開発に大きな展望をもたらすものと期待されます。ミクログリアの活性制御に特化した薬剤の開発を推進することにより、将来的に認知症の根本的な治療法を確立できる可能性があり、その際にミクログリアの活性レベルをPETで定量することで、臨床でも治療効果の評価が行えるようになると見込まれます。
用語解説
*1)認知症モデルマウス
アルツハイマー病をはじめとする認知症では、タウ蛋白と呼ばれる分子が病的線維を形成して神経細胞内に蓄積し、神経細胞死が起こることが知られています。このタウ蛋白の蓄積と神経細胞死を再現した遺伝子改変マウスが本研究で開発されました。
*2)ミクログリア
脳内では神経細胞の他に、グリア細胞と呼ばれる細胞が脳の形態や機能を維持するのに役立っています。ミクログリアは脳内の免疫反応などを担当する細胞で、この細胞の過剰な活性化は脳の損傷を加速することが示唆されています。
*3)PET
ポジトロン断層撮影(positron emission tomography)の略称で、生体の生理機能や病的変化を画像化する有力な手段として近年注目されています。また、最近ではマウスのような小動物の生体イメージングを可能にする高分解能PETが開発され、放射線医学総合研究所でも基礎研究に活用しています。
*4)トレーサー薬剤
PETによる生体イメージングは、放射性アイソトープで標識された薬剤を生体に投与し、PET装置により放射線を検出することで実現します。この時に投与する薬剤がトレーサー薬剤(あるいは分子プローブ)と呼ばれ、薬剤の分布・結合特性により生体の特定の分子や事象を画像化することが可能です。
*5)タウ蛋白
タウ蛋白は神経細胞の骨格を形成する分子の一つですが、アルツハイマー病などの認知症ではこのタウ蛋白が過剰にリン酸化された状態で神経原線維変化と呼ばれる線維状の病変を形成します。近年タウ蛋白の遺伝子異常が家族性の認知症をもたらすことが見出され、タウ蛋白が認知症の原因物質の一つであることが証明されてきています。
*6)DAA1106
放射線医学総合研究所が大正製薬(株)及び日本農薬(株)と共同でPETトレーサーとして開発した薬剤で、活性化ミクログリアに多く含まれる末梢性ベンゾジアゼピン受容体に結合する特性を持つことより、ミクログリアの活性上昇を画像化する上で有用な化合物です。
本件の問い合わせ先
独立行政法人 放射線医学総合研究所 広報室
Tel:043-206-3026
Fax:043-206-4062
E-mail:info@nirs.go.jp
