放医研、独自の超高比放射能合成技術により
脳内ドーパミンD2受容体に新たな超高親和性結合部位を発見
概要
独立行政法人放射線医学総合研究所(理事長:米倉 義晴、以下、放医研)分子イメージング研究*1センター分子認識研究グループの張 明栄チームリーダーらは、この程、PET診断を飛躍的に高感度化する高比放射能合成技術によって得られた超高比放射能のドーパミンD2受容体リガンド*2である[11C]ラクロプライド*3を用いた動物実験を行い、ラット脳の大脳皮質*4と線条体*5において、これまで見出されていた神経伝達を行う結合部位の他に、新たな超高親和性結合部位が存在することを発見しました。
PET(陽電子断層撮像法)を用いた研究では、通常用いられる標識薬剤の比放射能より桁違いに高い超高比放射能のリガンドを用いることにより、薬剤の生理活性による生体への影響を極限まで抑えることが可能となります。張らの研究は、従来に比べ1,000倍低いリガンド濃度による測定が可能になったことにより、極低濃度領域に神経伝達を行う新たな結合部位を見出したもので、生体内で起きる生命現象を解明する研究において、測定データを飛躍的に精緻化する世界で初めて明らかにされた成果です。
今回の成果は、国際核医学誌NUCLEAR MEDICINE AND BIOLOGY 35電子版2008(19-27)に掲載されました。
背景
放医研の分子イメージング研究センターは、卓越した分子プローブ合成技術を有し、中でも特に世界水準を大きく凌駕する超高比放射能のリガンドを合成する技術は、幅広いPET診断や研究を高感度で遂行することを可能にするもので、国内外の注目を浴びています。
比放射能とは、ある標識化合物の一定量(μmolまたはμg等)当たりどれだけの放射能(CiまたはGBq等)が含まれているかを示す指標です。半減期20分の11C標識薬剤の場合、理論的には1pmol(分子量100として1mgの千万分の一)で一人分のPET検査が可能な量となりますが、実際には環境中に含まれる大量の炭素により希釈され、通常得られるのは理論値の一万分の一程度となり、その分、測定に役立たない不要な化合物が投与されることになります。このような高い比放射能を有する標識化合物を合成するには、極めて高度な技術が必要ですが、放医研では鈴木和年分子認識研究グループリーダーを中心に長年研究開発を行い、現在では、世界水準の10~100倍高い比放射能を達成しています。
このような高比放射能リガンドを用いることにより、生体内にきわめて低濃度にしか存在していない分子などのイメージングが可能になります。また、結果的に投与する化合物(PET薬剤)を減らすことができることから、強い生理活性や毒性を有する薬剤でも生体に影響を与えることなくイメージングが可能となります。今回、超高比放射能リガンドの優位性を検証するため、ドーパミンD2受容体リガンドである[11C]ラクロプライドを用いたラット脳のイメージングを行いました。
研究手法と結果
張らは、広濃度範囲の[11C]ラクロプライド(0.3pM-18nM)を用い、ラット脳の線条体及び大脳皮質のホモジネート*6に対する結合実験を行いました。その結果、超高比放射能リガンドを使用することにより、通常のリガンド濃度より1000倍低い濃度での結合実験を実施することができ、線条体と大脳皮質において[11C]ラクロプライドが、異なる親和性を示す二つの部位に結合することを確認しました(図1)。
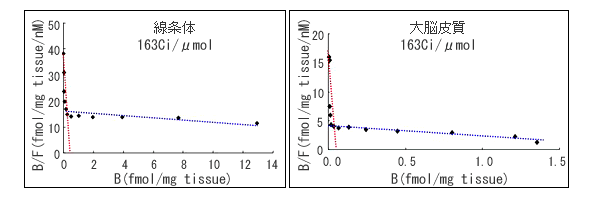
(図1)ラット脳の線条体及び大脳皮質のホモジネートに対する結合実験
超高比放射能薬剤[11C]ラクロプライドを使用し、通常のリガンド濃度より1000倍低い濃度で測定。ラットの線条体と大脳皮質において、それぞれに異なる親和性を示す二つの結合部位(赤、青で示す2つの点線)を確認した。
一方、あらかじめ非放射性D2リガンド*7をホモジネートに加えた結合実験では、線条体及び大脳皮質とも、それぞれ一つの結合部位しか確認できませんでした(図2)。
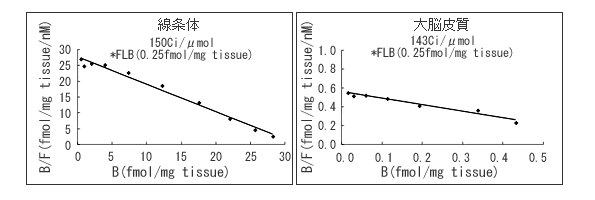
(図2)非放射性D2リガンドを加えたラット脳の線条体及び大脳皮質のホモジネートに対する結合実験
あらかじめ高い親和性をもつ非放射性D2受容体リガンドを加え高親和性部位を占有させた場合では、線条体及び大脳皮質にそれぞれ一つの結合部位のみを確認した。
100-200Ci/μmolの高比放射能を持つ[11C]ラクロプライドを使用し、ラット脳切片のARG測定を行いました。その結果、脳画像は比放射能が高い方がより鮮明で、通常の比放射能(1Ci/μmol)に比べ、高比放射能では線条体で3倍、大脳皮質で2倍の放射能集積を確認しました(図3)。
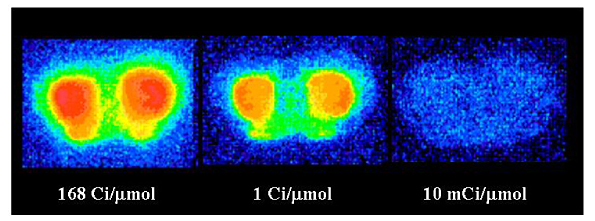
(図3)高比放射能薬剤(左)と通常比放射能薬剤(中)との集積比較
高比放射能[11C]ラクロプライドでは線条体で3倍、大脳皮質で2倍の放射能集積が増加し比放射能が高い方がより鮮明であることを確認した。一方、低比放射能(右)では、脳組織における放射能集積が消失した。
以上の結果、今回見いだされた結合部位は、通常のPETで用いられる標識薬剤の比放射能では見出すことのできなかった新たな結合部位である可能性が極めて高いことが示唆されました。また、高比放射能薬剤を用いることによって、より精度の高い画像が取得できることも明らかになりました。
期待される成果と今後の展望
放医研では、11C(炭素11)標識薬剤のほか、13N(窒素13)、18F(フッ素18)等の標識薬剤についても100Ci/μmol以上の超高比放射能を達成しており、PETを用いた研究や診断において、多種多様な超高比放射能を有するPETリガンドを利用することが可能となっています。これによって、神経受容体のような存在量が極めて少ない生体内分子のイメージングにおいても、高い特異結合/非特異結合比で感度よく測定することが可能となります。また、生理活性や毒性が強く生体への影響が大きいことから現在まで使用できなかった薬剤でも、超高比放射能リガンド化により、超微量での測定が可能となり、また、生体内に極低濃度でしか存在しない結合部位のイメージングなどの分子イメージング研究に新たな展開をもたらすものと期待されます。
用語解説
*1 分子イメージング研究
生体内で起こるさまざまな生命現象を外部から分子レベルで捉えて画像化することであり、生命の統合的理解を深める新しいライフサイエンス研究分野。PETによる腫瘍の診断もその一分野である。
*2 ドーパミンD2受容体リガンド
中枢神経系に存在する神経伝達物質であるドーパミンD2受容体と特異的に結合する化学物質の総称。
*3 [11C]ラクロプライド
ベンザマイド系の抗精神薬ラクロプライドの11C標識体でドーパミンD2受容体測定用の、標準的なPET用標識薬剤。選択性が高くD2受容体との結合はPET測定時間内に平衡に達し、次第に結合を解いていくことから、薬剤分布の時間変化を解析することにより、結合と解離の速度定数を求めることができる。
*4 大脳皮質
大脳の表面に広がる神経細胞の灰白質の層である。大脳基底核と呼ばれる白質の周りを覆っている。知覚、随意運動、思考、推理、記憶など、脳の高次機能を司る。
*5 線条体
線条体は、終脳の皮質下構造であり、大脳基底核の主要な構成要素のひとつ。運動機能への関与が最もよく知られているが、意思決定などその他の認知過程にも関わると考えられている。
*6 ホモジネート
生物の組織や細胞をホモジナイザーですりつぶして細胞の構造を破壊して得られる懸濁液。
*7 非放射性D2リガンド
放射性核種で標識した放射性D2受容体リガンドと区別して、放射能を持たないD2受容体リガンドを指す。
本件の問い合わせ先
独立行政法人 放射線医学総合研究所 企画部 広報室
Tel:043-206-3026
Fax:043-206-4062
E-mail:info@nirs.go.jp
