遺伝性小頭症遺伝子ASPM、
放射線の照射によって遺伝子発現が減少
-被ばくによる小頭症発症に関与か?-
概要
放射線医学総合研究所(理事長:米倉義晴;以下、放医研)重粒子医科学センター粒子線生物研究グループ(岡安隆一グループリーダー)の藤森亮・細胞分子機構研究チームリーダーらは、その機能喪失が遺伝性小頭症の原因である「ASPM遺伝子*1」が、人やマウスの細胞への放射線の照射によって、発現が抑制されることを発見しました。
小頭症のうち、遺伝性小頭症については、2つあるASPM遺伝子が共に機能しない場合、遺伝子産物であるASPM蛋白質の減少により小頭症の胎児が生まれることが明らかとなっていましたが、妊娠中の母胎の風疹感染や、胎児の放射線被ばく等の後天的要因によるものについて、そのメカニズムは完全に解明されたわけではありません。
今回、藤森チームリーダーらは、このASPM遺伝子の発現が放射線の照射によって顕著に減少することを突き止め、放射線被ばくによる小頭症の発症にASPM遺伝子が深く関与する可能性を新たに示しました。
本成果は、平成21年2月27日に開催いたします、「放射線医学総合研究所・粒子線生物ワークショップ」にて発表いたします。
背景
小頭症は、原爆症としても知られるように、胎児期の放射線被ばくが原因の典型的な発達障害ですが、放射線被ばくがなぜ脳の発達を妨げるのかという点については解明されていません。
一方、放射線被ばくのような後天的要因によるものではなく、遺伝的に発症する家族性小頭症(劣性遺伝病)(図1)については、近年その原因がASPM遺伝子の機能喪失によるものである、ということが確認されています。
ASPM遺伝子は、胎児の大脳を形成する時期の未分化な神経前駆細胞*2において強く発現します。このことから、その時期の発現が抑制されることによって小頭症が生じる可能性があると考えられていましたが、この遺伝子と放射線の関係についてはまったく判っていませんでした。
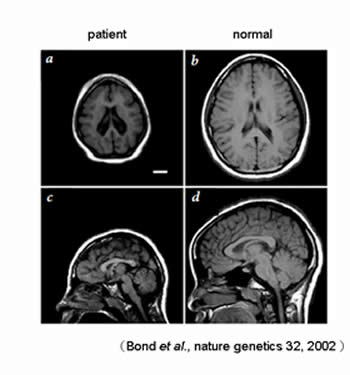
図1 家族性小頭症患者の頭部CT画像
(a,c)患者の頭囲は明らかに小さく、本症例では精神遅滞を伴う。
右(b,d)が正常な患者のもの。
この要因はASPM遺伝子の機能喪失によるものである。
研究手法と成果
胎児性ヒト線維芽細胞に放射線(X線または治療に用いる炭素イオンビーム)を照射し、約16,000の遺伝子を対象としてHiCEP法*3を用いた非照射サンプルと照射サンプルの遺伝子発現量を比較しました。その結果、放射線に曝露された細胞でいくつかの特定の遺伝子の発現が、比較的短時間(4時間)のうちに増加または減少しました。この中で、明確に発現抑制を観測することができた遺伝子のひとつが、家族性小頭症に関係するASPM遺伝子であることが判明しました(図2、図3)。
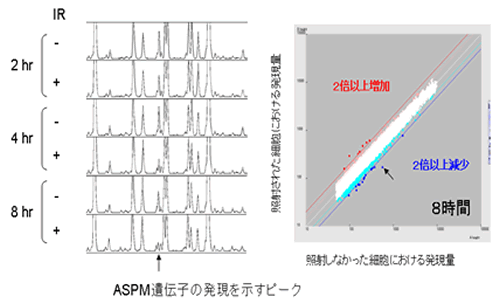
図2 放射線によって発現が変動する遺伝子の検出結果
ヒト胎児肺線維芽細胞にHIMAC炭素イオン線2Gy(70keV/μm、高LET)を照射し、2、4、8時間後にRNAを抽出して遺伝子発現プロフィールを作製した(左)。照射サンプルと非照射サンプルのデータを網羅的に比較することによって、ASPM(矢印)が抽出された。
ASPM遺伝子は、細胞分裂を繰り返し増殖する細胞(特に神経前駆細胞)の分裂において働くASPM蛋白質をコードする遺伝子で、遺伝性小頭症の患者ではこのASPM遺伝子に様々な変異が生じており、変異遺伝子から合成されるASPM蛋白質の機能の低下が胎児に小頭症を引き起こすことが分かっていました。
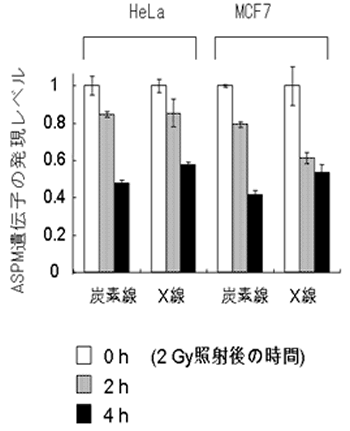
図3
放射線によるASPM遺伝子発現の減少は、HeLa(子宮がん由来)、MCF7(乳がん由来)などヒトのがん由来の培養細胞においても見られた。
マウスにもこのASPM遺伝子に相当する遺伝子(Calmbp1)が存在し、胎児期から出生後の間に中枢神経の発生・発達に関連した発現を示します。妊娠マウスで行ったX線(2Gy)照射実験で、ASPM遺伝子の発現の減少は、神経前駆細胞が多数存在する脳室下領域(SVZ)で起こっていることを確認することができました。
さらに胎児から回収して培養した神経幹細胞(神経細胞またはグリア細胞に分化する前の未分化な細胞)では、mRNA(蛋白質に翻訳され得る塩基配列情報と構造を持ったRNA)と蛋白質のレベルで、放射線が同遺伝子発現を劇的に減少させていることも明らになりました(図4、図5)。
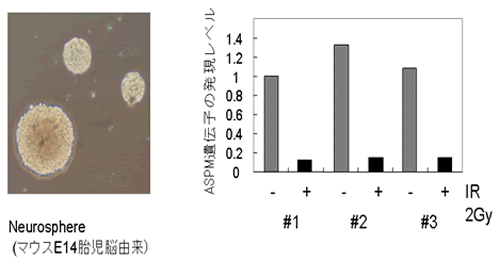
図4 被曝したマウス神経幹細胞におけるASPM遺伝子発現の著しい減少結果
左は、マウス神経幹細胞の培養系(neurosphere)。X線(2Gy)をこれに照射し、その2時間後にRNAを抽出し、マウスASPM遺伝子発現を調べた。
右は、3回の独立の実験の結果(-照射なし、+照射あり)。
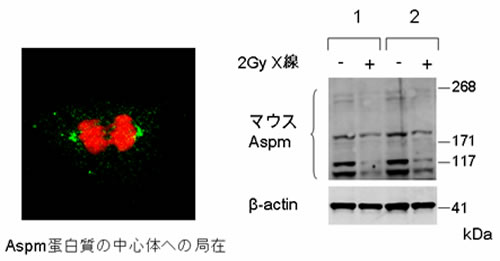
図5 マウスASPM蛋白に対する抗体を用いた実験
左はマウス胎児線維芽細胞の有糸分裂期の顕微鏡写真。染色体は赤色、ASPM蛋白質は抗体(緑色)で標識した。右は、X線を照射したneurosphere(図4)から3時間後に蛋白質を抽出し、ASPM蛋白質の減少をウエスタンブロットで解析した、独立の2回の実験を示す(-照射なし、+照射あり)。
ASPM遺伝子は胎児の大脳形成に伴い、未分化な神経前駆細胞で強く発現します。このため、遺伝性の小頭症だけに限らず、放射線などの後天的要因によって起こる(非遺伝的)な小頭症もまた、同遺伝子の機能抑制によって生じる可能性は十分考えられ、今後さらに詳しい研究が必要ではあるものの、放射線被ばくによる小頭症発症のメカニズムに関する新たな一つの説として興味がもたれます。
今後の展開
家族性小頭症関連遺伝子は、ASPMを含めて現在6つ同定されており、それらの機能はいずれも細胞分裂時の紡錘体形成に関係しています。これらの細胞分裂機構は近年、がん治療の標的としても注目されています。また、海外の研究グループからは、ASPMと同じく家族性小頭症関連遺伝子に属するMCPH1(microcephalin)の遺伝子産物がDNA損傷に対する生体応答機構に関わることが報告されています。
このように、小頭症原因遺伝子の放射線生物効果に関する機能研究は今後、放射線治療学やその他の分野で発展することが期待されており、藤森チームリーダーらは、放射線に対するASPM遺伝子の応答等について、さらに研究を進めています。
用語解説
*1:ASPM遺伝子
abnormal spindle- like microcephaly associated gene(異常紡錘体様小頭症関連遺伝子)の略名。ヒトの脳の大脳皮質の発達に重要な役割を果たしたと考えられる遺伝子であり、ヒトを含む霊長類のASPM遺伝子の塩基配列を比較することにより、ヒトへと進化する霊長類の遺伝子変化に関する研究に用いられている。ヒトのASPMは最近クローニングされ、もっとも一般的なタイプの家族性小頭症(MCPH5)の原因遺伝子であることが証明された(Bond et al.Nat.Genet.2002)。
*2神経前駆細胞
脳を構成するニューロンやグリア細胞等の主要な細胞に分化する能力と増殖する能力を持つ未分化な細胞。
*3:HiCEP(高カバー率遺伝子発現プロフィール解析技術)
本研究所の重粒子医科学センター先端遺伝子発現研究グループ(安倍真澄グループリーダー)が開発した網羅的遺伝子発現解析技術。遺伝子発現の際に作られるmRNA分子から人工的に合成したDNA分子(cDNA)を、制限酵素(DNAの特定の塩基配列を認識して切断する酵素)で切断し、切断されて残ったcDNA分子の長さで遺伝子の種類の違いを区別し、それぞれの発現量を蛍光強度などに置き換えて定量するAFLPを原理とする。HiCEPは、技術改良によってこれに分解能・検出感度・再現性を補い、発現プロフィールの重ね合わせによって遺伝子発現の比較定量を可能にした方法で、細胞内の全転写産物の最大70~80%を網羅する「高いカバー率」を達成したことから、High-Coverage Expression Profiling=HiCEPと名付けられた。同法の高カバー率・高感度の利点を活かし、ヒトの培養細胞における低線量の放射線に応答する遺伝子の同定に成功した例や同法が遺伝子応答の探索に遺伝子塩基配列情報を必要としないことの利点を活かし、土壌生物トビムシの放射線応答遺伝子の同定に成功した例などがある。
問い合わせ先
国立研究開発法人 放射線医学総合研究所 企画部 広報課
Tel:043-206-3026
Fax:043-206-4062
E-mail:05;nfo@nirs.go.jp
