小動物生体イメージングを用いた
抗うつ薬薬効評価システムを開発
―創薬効率の飛躍的向上へ前進―
概要
独立行政法人放射線医学総合研究所(理事長:米倉義晴、以下、放医研)分子イメージング研究センター分子神経イメージング研究グループ(須原哲也グループリーダー)分子生態研究チームの樋口真人チームリーダー、西條武明客員協力研究員らは、陽電子断層撮影(PET*1)装置を用いて抗うつ剤(うつ病の治療薬)が脳内の標的分子に結合する割合を、小動物(ラット)で測定することにより、その薬剤がヒトで効果を発揮するのに必要な量を高精度に予測できることを世界で初めて明らかにし、さらに新規抗うつ薬候補物質と既存の薬剤の生体内での効果の比較を、小動物でヒトと同様に行うことに成功しました。
これらの結果は、小動物を使ったPETイメージング技術が、薬剤開発の初期段階における、薬の特性やヒトに投与する際の効果をいち早く知ることを可能にし、わが国の企業が創薬において国際的にも高い競争力を発揮するための強力な手段を提供しえます。
本研究は放医研および田辺三菱製薬株式会社の共同研究による成果で、雑誌「International Journal of Neuropsychopharmacology」2009年2月23日号に掲載されました。
研究の背景と目的
医薬品の創製・開発において、臨床試験の成功率が低いことは製薬企業において大きな問題となっています。医薬品候補化合物は、実験動物を用いて詳細に薬の効果、安全性などを検討し、ようやく臨床試験を行うことができます。ところが臨床試験に到達した医薬品候補化合物の実に90%以上が開発の中止を余儀なくされています。その主な原因の1つが「実験動物で得られていた薬の効果が臨床試験で十分に得られなかった」というものです。特に精神疾患に関しては、病態動物モデルは数多く提唱されているものの、薬を投与した後の動物の行動を評価するだけではヒトでの効果を予測することが難しく、実験動物を用いる評価とヒトでの臨床試験の結果との間に大きな「ギャップ」がありました。
うつ病のような精神疾患に対する治療薬の多くは、脳内の標的分子に結合することでその効果を発揮すると考えられています。これらの標的分子の多くは実験動物とヒトに共通して発現していることから、実験動物で医薬品候補化合物が標的分子に結合する割合を指標化(「占有率」)し、評価することで、ヒトでの効果を高精度に予測可能となることが期待されます。PET測定は非侵襲的に脳内の標的分子に対する治療薬の占有率測定を可能にし、客観的に薬の効果を予測、判定することができる非常に有用な手法です。ラットやマウスのような小動物の脳内を高解像度で撮像可能とするPET装置の開発によって、小動物を用いたヒトでの薬効予測が現実的なものとなってきました。
本研究では、脳内のセロトニントランスポーター*2に結合することでうつ病治療効果を発揮する抗うつ剤として、既に医薬品として上市されているフルボキサミン*3や、新規抗うつ薬候補であるWf-516をラットに投与し、脳内セロトニントランスポーターへの結合占有率をPET測定によって算出しました。これによって得られたデータを、ヒトのPETデータやラットから摘出した脳のデータと比較することで、小動物PET測定が薬剤の前臨床開発に役立つシステムとなりうるかどうかを検討しました。
研究手法と結果
本研究ではラットにWf-516またはフルボキサミンを内服させ、セロトニントランスポーターに選択的に結合するPETトレーサーである[11C]DASBを静脈注射してPET撮影を行い、薬物による脳内のセロトニントランスポーターへの占有率を測定しました。薬物を投与せず[11C]DASBのみを投与した場合、脳内のセロトニントランスポーターへ結合できるのは、脳内で合成された神経伝達物質セロトニンと体外から投与された[11C]DASBです。しかし、あらかじめWf-516やフルボキサミンを投与しておくと、これらもセロトニントランスポーターへ結合するため、相対的に[11C]DASBがセロトニントランスポーターへ結合する量が少なくなります。すなわち[11C]DASBの結合低下の割合を定量することによって薬物によるセロトニントランスポーターの占有率を算出することが可能になります(図1)。
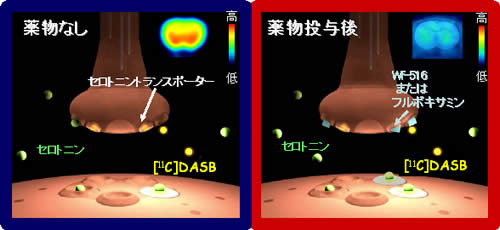
図1 PETを用いた脳内セロトニントランスポーター占有率測定
Wf-516またはフルボキサミンがセロトニントランスポーターに結合すると、[11C]DASBのセロトニントランスポーターへの結合が低下する。この低下の割合を定量することによって薬物による占有率が算出可能となる。
Wf-516およびフルボキサミンは、投与量に依存して[11C]DASBのラット脳内セロトニントランスポーターへの結合を低下させる、すなわち投与量を増すほどこれらの薬物がセロトニントランスポーターへ多く結合することがラット脳内のPET画像から明らかになりました(図2)。
![[11C]DASB を用いたラット脳内セロトニントランスポーターのPETイメージング画像](/uploaded/image/2440.jpg)
図2 [11C]DASBを用いたラット脳内
セロトニントランスポーターのPETイメージング画像
Wf-516およびフルボキサミンの投与量の増加に伴い[11C]DASBの線条体、視床および中脳(いずれも脳の深いところにある領域でセロトニントランスポーターを多量に含む)への結合が低下し、薬物がセロトニントランスポーターへ結合していることが目に見える形で確認された。
ラット脳内に[11C]DASBを投与後、放射能をPETで時間経過を追って解析し、薬物の占有率を算出しました(図3)。抗うつ剤の投与量が増すとセロトニントランスポーターへの結合も増すことが視覚的に示されましたが(図2)、ここでは同じ現象を定量的に確認できました。
また、セロトニントランスポーターを50%占有するときのWf-516の投与量(ED50値)はフルボキサミンに比べて約1/5で、Wf-516の方がフルボキサミンより少ない投与量で効果を発揮しうることも明らかとなりました。
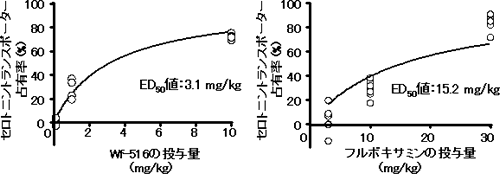
図3 Wf-516およびフルボキサミン投与後のセロトニントランスポーター占有率
フルボキサミンについては、ラットを用いてPET撮影時に採血を行って血中の薬物濃度を測定し、血中濃度と占有率の関係を調べました(図4)。セロトニントランスポーターを50%占有するときの血中フルボキサミン濃度(EC50値)は6.1ng/mLであり、放医研で過去に実施したヒトのEC50値(4.6ng/mL)と非常によく一致していることが明らかとなりました。
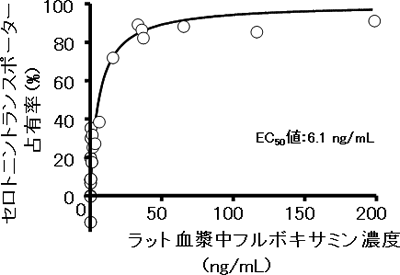
図4 ラット血漿中フルボキサミン濃度とセロトニントランスポーター占有率の関係
本研究成果と今後の展望
今回、PETを用いた薬物による標的分子への占有率測定が小動物とヒトとで強く創刊していることについて、セロトニントランスポーターを例として示すことができました。現在のところ、精神疾患治療薬の開発において、PET測定から得られる占有率は動物とヒトに共通する唯一の指標です。小動物を対象としたPET測定を前臨床期から取り入れることで、ヒトにおける薬物の効果を精度良く予測することができ、結果的に臨床試験の成功率の飛躍的向上に寄与できると考えられます。
また、このように臨床予測性の高い手法を用いて、Wf-516のような新規医薬品候補化合物とフルボキサミンなどの既に上市されている薬剤を比較するにより、新規薬剤が既存の薬剤よりも優れているかどうかを明確に評価することが可能になります。
さらにPETは生体で測定を行うため、同じ個体を用いて繰り返し測定することが可能です。これは従来の非臨床試験に比べて統計上のばらつきを小さくできるだけでなく、使用する動物数を劇的に減らすことにもなり、薬剤開発の効率が向上します。加えて、侵襲性が少ないことから動物の苦痛軽減にもなり、動物倫理の観点からも有利です。将来的には本研究によって確立した小動物PET測定技術を、様々な精神疾患治療薬開発で活用することにより、少ないコストで治療薬の早期臨床応用を実現するシステムがもたらされると見込まれます。
用語解説
*1 PET
Positron emission tomographyの略称。画像診断装置の一種で陽電子を検出することによって様々な病態や生体内物質の挙動をコンピューター処理によって画像化する技術。
*2 セロトニントランスポーター
神経細胞から放出されたセロトニンを細胞内に取り込むタンパク質。細胞外のセロトニン濃度の低下がうつ病の原因の1つとされており、フルボキサミンのようにセロトニントランスポーターに結合しセロトニンの再取り込みを阻害する薬剤は抗うつ効果を発揮すると考えられている。
*3 フルボキサミン
セロトニントランスポーターに選択的に結合し、セロトニンの細胞内への再取り込みを阻害する抗うつ薬。うつ病以外にも強迫性障害などの治療にも用いられる。
問い合わせ先
国立研究開発法人 放射線医学総合研究所 企画部 広報課
Tel:043-206-3026
Fax:043-206-4062
E-mail:05;nfo@nirs.go.jp
