概要
独立行政法人放射線医学総合研究所(理事長:米倉義晴;以下、放医研)重粒子医科学センターゲノム診断研究グループ(今井高志グループリーダー)の道川祐市主任研究員らは、両親から1本ずつ伝わる2本の染色体DNAの断片を1分子レベルで単離し、さらにそれぞれを10万倍程度まで増幅する技術の開発に成功しました。
これまでの試料採取方法では、両親由来の染色体DNAが混在してしまうため、ハプロタイプ(*1)多型の解析は困難でした。しかし本技術は200kb(*2)以上、最大800kbの長さ(従来の手法では20kb)で染色体DNAを単離でき、しかも高い増幅率を有することから、一般的で安価な解析手法を用いても高精度で、両親から伝わる2種類の遺伝情報を識別しながら解析できるようになりました。この技術開発により、遺伝性疾患の発症機構について新たな解明手法の開発を可能とし、安価で高精度の遺伝子解析が行えるようになる等、医学の発展に貢献することが期待されます。
本研究の成果は、平成20年12月15日発行の米国科学誌Analytical Biochemistry誌に掲載されます。また、平成20年11月21日に福岡県北九州国際会議場で開催される第51回日本放射線影響学会で発表いたします。
背景
人を含む多くの高等動物は両親から1対の染色体を受け継いできています(図1)。染色体を構成しているのがDNAですが、すべての染色体が同じDNA配列でできているわけではなく、染色体ごとに塩基の種類(A,C,G,T)が異なっています。またひとつの細胞内にある1対の染色体同士でも個人個人で(父親由来と母親由来とで)異なっています。これらの違いが、人の顔かたちや背の高さ、お酒に対する強さ、寿命の長さ、各種疾病への罹り易さなどを決めていると考えられています。近年、ヒトゲノム全塩基配列解読技術は格段に進歩を遂げており、近い将来10万円程度で個人のゲノム塩基配列の解読技術を開発して、医療に役立てようとする動きが加速しています。しかし、このように遺伝解析の重要性が年々増して、個人の膨大な遺伝情報を短期間で安価に解読する技術が求められるようになってきた一方で、両親から伝わる1対(2本)の染色体DNAは物理化学的性質がほぼ等しいため分離が困難であり、ヒトゲノム研究の多くにおいては、それらが混在したまま取り扱われることになり、染色体のDNA配列が両親のうち何れかを由来としているか特定できず、精度の高い解析が行えない等、ゲノム研究の妨げのひとつになっていました。
技術の概要
DNAをアガロースゲルの内部で1分子にまで希釈分散させることにより個々の染色体DNA断片を従来の手法より安定な状態で単離し、それをゲルに添加したDNAポリメラーゼ(*3)の作用によって10万倍程度まで増幅させるものです。この増幅させたDNAはアガロースゲルを加熱することで水溶液中に回収でき、特別な処理をすることなく、そのまま様々なゲノム研究に用いることができます。
技術の詳細
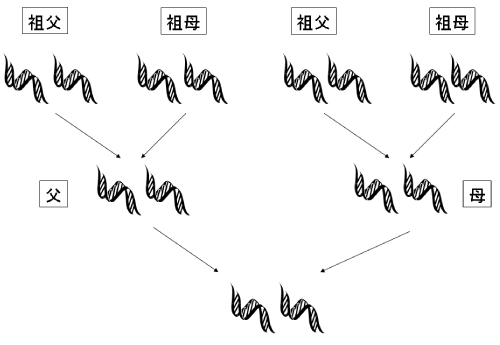
図1 両親からの遺伝情報伝達。子供は両親からそれぞれ半分の遺伝情報を受け継ぐ
全ての遺伝情報を解読するための技術が盛んな開発競争を繰り広げられている一方で、個人の中に存在する両親由来2種類の遺伝情報を識別して解読し、組み合わせを明らかにする技術はほとんど進展が見られていませんでした。上述した顔かたちや背の高さ、お酒に対する強さ、寿命の長さ、各種疾病への罹り易さというような表現型の違いは遺伝情報の塩基の違いに起因することが多いのですが、これまでの解析方法では、染色体DNAをミックスして取り扱っているため、多くの場合その塩基の違いが父親由来であるのか母親由来であるのかが不明でした(図2)。両者を識別しないまま全塩基配列を解読しても、個人の遺伝情報として完全ではありません。また最近の研究ではこのような塩基の違いをひとつのセットとしてもった染色体上のDNA断片(ハプロタイプ)の重要性が明らかとなり、このハプロタイプが父親由来か母親由来かを把握することが、より正確なゲノム研究や、さらには病気の罹りやすさを予測する方法の開発につながると考えられています。
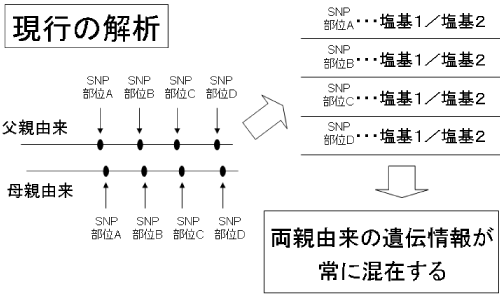
図2 現在開発が進められている遺伝情報解読技術。両親由来の対立遺伝子を識別することが困難なため、ミックスしたまま取り扱われている
本研究では両親由来の遺伝情報を識別するために、新しい解析技術を開発しました(図3)。この技術では染色体DNA断片が1分子レベルで単離された後に増幅されます。本技術を用いることで、これまで困難であった両親由来のハプロタイプを、区別できることが示されました。
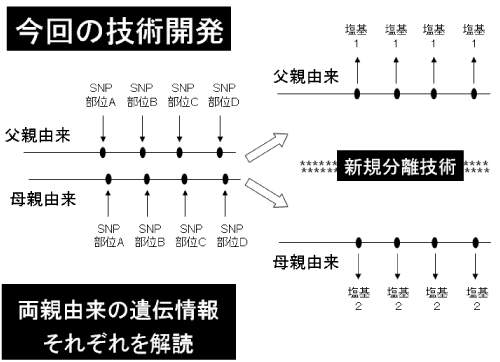
図3 本研究で開発された新しい遺伝情報解析技術。両親由来の染色体DNA断片を個別に増幅することで、両者がミックスされていない純粋な遺伝情報の解析が可能となった
研究手法と結果
本研究成果では、DNAをアガロースゲル担体の内部で1分子レベルにまで希釈分散させてからゲルを小容量ずつ分注することで、両親由来の染色体DNA断片が分離されます(図4)。その後にゲルに外から添加されたPhi29 DNAポリメラーゼ(*4)の働きによりそれぞれを10万倍ほどまで増幅できることが示されました(図5,6)。水溶液中でDNAを希釈分散させると、DNAが不安定化して細切れになったり、くっつきあったり、反応チューブに吸着するなど不都合なことが多くなります。それがアガロースゲル内部にDNAを埋め込むことで解消されることがわかりました。アガロースゲルはDNAのような巨大分子の出入りは妨げますが、酵素タンパク質やプライマー(*5)のような比較的小さな分子は自由に出入りが可能です。そのため、ゲル内部に埋め込まれたDNAでも外部から添加した酵素溶液により10万倍ほど増幅を行えます。増幅産物は加熱によりアガロースゲル内部から水溶液中に回収され、様々な解析に用いることができます。本研究では一例として、これまで両親由来染色体の混在により困難とされていたハプロタイプ多型の解析が示されました(図7)。
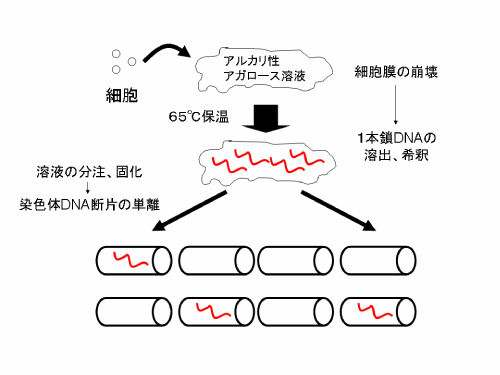
図4 アガロースゲルを用いた染色体DNA断片の1分子レベル単離。アルカリ性のアガロース溶液内で65℃に保温されることにより、細胞内のDNAは溶液中へ1本鎖に変性しながら希釈される。アガロース溶液を小容量ずつ分注することで中に含まれる染色体DNA断片が単離される
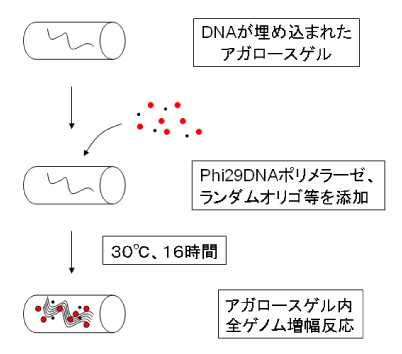
図5 アガロースゲルに埋め込まれた染色体DNA断片の増幅。ゲル内に埋め込まれたDNAは巨大分子であるため外部に漏出する可能性がほとんど無いが、酵素タンパク質やプライマーは自由に出入りすることができる。Phi29 DNAポリメラーゼは鎖置換型DNA合成活性(*6)を有し、温度サイクルを与えなくても一定温度(30℃)でDNA増幅反応を恒常的に行う

図6 ゲノム増幅反応後のアガロースゲル比較。ゲルの内部でゲノム増幅反応が行われたことで色素に染まるようになり、非常に強い蛍光を発するようになった(左側、反応+)
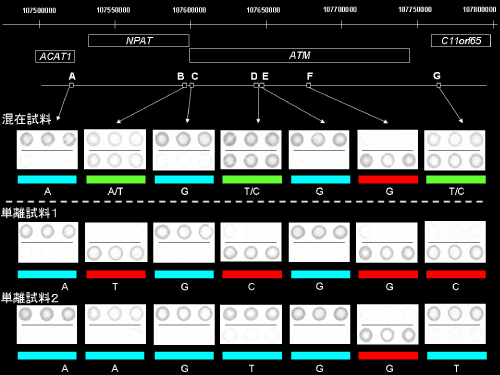
図7 ハプロタイプ解析例。両親由来染色体DNAが混在している試料において3箇所存在していたヘテロ接合型(緑)が、単離試料では全てホモ接合型(赤もしくは青)になっている。この検体は2種類のハプロタイプ(A-T-G-C-G-G-C、A-A-G-T-G-G-T)を有することが判明した。各塩基の解析結果は上段と下段にそれぞれの塩基を識別するスポットが3連ずつ示されている
本研究の成果と今後の展望
本研究成果により、両親由来の染色体DNA断片を個別に単離してそれぞれの遺伝情報を解析できることが示されました。今回の研究では単離した染色体DNA上に存在するハプロタイプ多型の解析を行いましたが、今後は技術開発を進めて連続的な塩基配列を解読できるようにする予定です。本研究成果を用いて、両親から伝わる2種類の遺伝情報をそれぞれ識別しながら解読する新たな道が切り開かれることで、完全なヒトゲノム解読が可能になると考えられます。これまではひとつの核内に存在する1対の染色体がそれぞれどのように役割分担をしているのかあまり理解されずにいましたが、両者を識別することにより新たな遺伝性疾患の発症機構が解明され、医学のさらなる発展に貢献する可能性が期待されます。
用語解説
*1 ハプロタイプ
ハプロイドジェノタイプ(半数体の遺伝子型)の略。父親もしくは母親に由来する単一染色体上のひとつながりの遺伝子構成。限定的に同一染色体上で遺伝的連鎖している多型の組み合わせのことをいうこともある。ハプロタイプを調べることでどちらの親から引き継がれた染色体かがわかるため、様々な疾病の家系調査に有用である。
*2 b(ベース)
bは、1本鎖DNAの塩基の長さを表す単位。1bは塩基と塩基の間の距離で、0.34nm。
*3 DNAポリメラーゼ
1本鎖のDNAを鋳型として、それに相補的な塩基配列を持つDNAを複製して2本鎖とする酵素の総称。鋳型を必要とせず一からDNAを新規合成できるDNAポリメラーゼはこれまで知られていない。一部のウィルスを除く全ての生物に存在する。
*4 Phi29 DNAポリメラーゼ
枯草菌(通性嫌気性の桿菌)に寄生するPhi29ファージ(細菌類を攻撃するウィルス)から精製されたDNAポリメラーゼ。最適温度は30℃。DNAを複製する際のエラーが非常に少ないことと一度に長いサイズのDNAを複製できるため、近年ごく微量のゲノムDNAを大量に増幅する目的で盛んに利用されてきている。
*5 プライマー
DNA複製の開始反応に要求されるDNA分子。鋳型となる1本鎖DNAに相補的に結合した後に、その3’側末端に対して新しい塩基が順次付加される形で複製反応が開始される。
*6 鎖置換型DNA合成活性
鋳型DNAに相補的なDNA鎖を合成していく過程で、伸長方向に2本鎖領域があっても合成反応を中断させず、障壁となる2本鎖を引き離しながら、相補鎖合成を継続する酵素活性。この活性を持つ酵素はPCR反応のような温度サイクルを必要としない。
問い合わせ先
独立行政法人 放射線医学総合研究所 広報課
Tel:043-206-3026
Fax:043-206-4062
E-mail:info@nirs.go.jp
