【高磁場磁気共鳴画像法による細胞・分子イメージング研究】
脳梗塞の後に起きる「神経膠(こう)症」の
高分解能イメージングに成功
~脳梗塞治療薬や神経再生医療の開発に貢献~
独立行政法人放射線医学総合研究所(理事長:米倉 義晴)
分子イメージング研究センター※1(菅野 巖 センター長)
青木 伊知男 チームリーダー
明治国際医療大学※2、田中忠蔵教授、河合裕子助教
米国国立衛生研究所・国立神経疾患脳梗塞研究所※3Afonso C Silva博士
成果の概要
高磁場磁気共鳴画像(MRI)※4と細胞内に取り込まれる機能性造影剤を用いて、脳梗塞で生じる神経膠症(グリオーシス)※5が梗塞の周辺部位で増大する様子を、世界で初めて、生きたままのラットの脳で、高い分解能で画像化することに成功しました。これは、医療現場で使用されている経口造影剤と同じ成分のマンガン造影剤とMRIを用い、マンガンイオンが効率的に神経膠症の原因であるグリア※6細胞内に取り込まれる事を発見・活用したことによるものです。
この技術は、脳梗塞の治療薬や神経を再生する技術を開発する場合に、神経膠症を生きたままの脳で、従来の50~100倍もの分解能で画像化できる点で画期的です。実験動物を用いて治療薬の薬効を迅速に評価可能になるために開発が加速でき、将来的には神経幹細胞移植の効果判断、脳梗塞の早期発見にもつながると考えられます。
この成果は、脳・神経科学において有名な米国の専門雑誌『NeuroImage』の2月15日号(49巻4号3122-3131頁)に掲載され、またオンライン版も公開されています。
成果のまとめ
これまで、動物実験において、脳梗塞を引き起こす神経膠症(グリオーシス)の発生を確認するには、死後に脳を摘出し、薄い切片を作成して顕微鏡で観察する方法しかなく、グリオーシスの状態を正確に把握することが出来ませんでした。
今回の研究では、マンガンイオンが効率的に高い密度と活性を持つグリア細胞内に取り込まれる事を発見し、ラットの脳梗塞の実験モデルを用い、生きたまま脳のMRI(磁気共鳴画像)を撮影することで、傷害部位を取り囲むように発生した神経膠症(グリオーシス)を、白い信号として画像で検出することに成功しました(図1)。
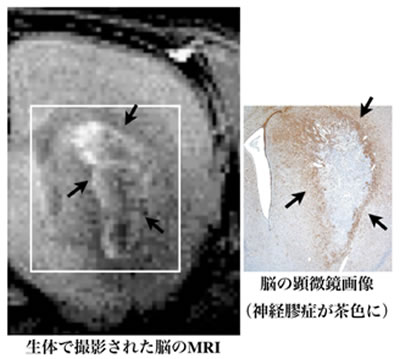
(図1)MRI像(左)では脳梗塞が起きた場所を取り囲むように環状に白く造影された。死後の組織染色像(右)と比較して、その部位が神経膠症であることを確認した。高磁場MRIでは、脳梗塞の傷害部位を100ミクロン程度の精度で画像化できる。
この研究は、機能性造影剤の技術と高磁場MRIを用いることで、脳梗塞後に発生した神経膠症(グリオーシス)を0.1mm程度の高い分解能(これまでの手法では5~10mm程度)で画像化した世界で初となる研究成果です。撮影には、医療現場で広く使用されているMRIを用いるので、CT撮影などに使われる放射線の照射や投与は不要です。今後、本研究によって開発した技術は、アストログリア※7の増殖を制御する脳梗塞や神経外傷の治療技術の開発に繋がります。また、新しい原理による脳梗塞治療薬の開発や、iPS細胞やES細胞の研究で注目される神経幹細胞を移植することで、神経の再生を促す技術の開発など、幅広い医療・医薬品開発分野への貢献が期待できます。
1.背景
脳梗塞(一般には脳卒中とも言われる)は、日本人の死亡要因で10.3%(第3位)を占め、2007年時点での脳血管疾患は、年間6万人を超えるほど社会的に重大な病気です。最近では、脳梗塞の治療法として血液の固まりを溶かす薬剤(血栓溶解療法)が登場しましたが、発症直後にしか利用できないことに加え、脳内出血が起きる危険性があるなどの理由から、多くの症例に適用されていません。脳梗塞は、早期に治療が開始できなければ、その障害を軽減するための効果的な治療法はないのが現状です。将来的には、失われた神経細胞を移植治療などにより「再生」させるという積極的な治療が期待されていますが、まだ解決すべき問題点が多く残ります。
効果的な治療法の鍵になるのは、神経膠症(グリオーシス)の発生です。脳梗塞に限らず、脳や脊髄に大きな傷害を受けると、グリア※6と呼ばれる細胞が傷害部位に集まったり、傷害部位で増殖したりする現象が起きます。アストログリア※7は、グリア細胞の一種で星状膠細胞とも呼ばれ、正常な状態では神経の保持や、血液から脳に取り込む物質の交換に関与する細胞です。脳に障害が起きると、このアストログリアが過剰に増殖して、場合によっては神経の回復を妨げ、再生医療を行う際に、移植した細胞の発育を邪魔する存在とされてきました。しかし、一方では傷害時に起こる炎症が脳全体に広がるのを抑えるために、「防波堤」のようなバリヤーを形作り、脳を守っているという研究もあります。つまり、神経膠症(グリオーシス)は、良い面と悪い面を併せ持つ諸刃の剣であり、必要なときに炎症を抑え、必要なときに神経再生を邪魔しないように「制御」することが脳梗塞の治療に重要だと考えられます。これまでの技術では、この神経膠症(グリオーシス)を生きたまま観察することはできなかったので、対策を立てることも、治療薬の効果を確認することも困難でした。
2.研究手法と成果
研究グループは、脳梗塞で生じた神経膠症(グリオーシス)を可視化するため、MRI(磁気共鳴画像)の造影剤の一つであるマンガン造影剤に注目しました。神経膠症の原因であるグリア細胞は、細胞が活発で密度が高いという特徴を持ちます。マンガン造影剤が、細胞活性と密度が高いグリア細胞に多く取り込まれるのではないかと仮説を立てました。
麻酔下のラットを対象に実験的な脳梗塞を作成し、この脳梗塞モデルのラットに対してマンガン造影剤を使用しました。約3週間の間、脳の変化を高磁場MRI※7を使って画像化しましたところ、梗塞の発症から10日目以降に、神経の傷害部位を取り囲むような白い信号(信号上昇)が見られました(図1)。死後に神経膠症部位を組織染色して、比較することで、この信号上昇が見られた部位が神経膠症の起こっている場所であることを確定しました。つまり、マンガン造影剤がグリア細胞に多く取り込まれることをつきとめ、そのMRIでの撮像に成功したことを意味します。
3.今後の展開
今後、本研究の成果である「生きたまま、グリオーシスを観察できる技術」は、脳梗塞によって生じる細胞レベル・分子レベルでのメカニズムの解明、脳梗塞の治療薬の開発や改良、神経再生医療を生体に応用する際の基礎研究に大いに役に立つと考えられます。また、動物を生きたまま観察できるため、より迅速かつ低コストで新しい治療薬を開発する事に貢献できます。
この技術は、現時点では、そのまま直接人体や患者に応用することは出来ませんが、使用した機能性造影剤と同じ成分が、経口造影剤として消化管造影などに医療現場で使用されています。また、医療現場で広く使用されているMRIを利用しています。このため新しい薬剤送達技術や造影剤合成技術を融合することで、より安全性の高い手法に繋がると考えており、今後、安全性や造影効果の向上などの改良を行う予定です。
本研究は“生体内で起こる様々な生命現象を外部から分子・細胞レベルで捉えて画像化する”分子イメージング技術の一種です。放医研・分子イメージング研究センターでは、では今後も臨床応用を目指した革新的なイメージング技術の開発に取り組んでいきます。
用語解説
※1 分子イメージング研究センター
平成17年度に放医研に創立された分子イメージング研究を行っている研究センター。腫瘍や精神疾患に関する基礎研究や臨床研究のほか、分子プローブの開発や放射薬剤製造技術開発、PET開発やMRIの計測技術開発など、分子イメージングの基礎研究から疾患診断の臨床研究まで幅広い研究を行う世界屈指の分子イメージング研究拠点。文部科学省が推進する「分子イメージング研究プログラム」の「PET疾患診断研究拠点」として選定を受けている。
※2 明治国際医療大学
明治国際医療大学は、明治鍼灸大学を前進とする医療系大学であり、鍼灸学部に次いで柔道整復学部・看護学部が開設されている。「附属病院」「メディカルMRセンター」「附属鍼灸センター」など7施設が併設され、臨床実習教育や専門教育に力を入れている。統合医療の発展を目的に、臨床研究や基礎研究が行われている。
※3 米国国立衛生研究所・国立神経疾患脳梗塞研究所
世界最大の規模を誇る米国の国立医学研究所群(National Institutes of Health (NIH))において脳神経障害の研究を行う国立研究所(National Institute of Neurological Disorders and Stroke(NINDS))。動物実験用11.7テスラ超高磁場MRIやヒト用7テスラ高磁場MRIを保有し、イメージング研究をリードしている。
※4 高磁場MRI
より高い磁場ほど強い信号が検出できるが、安定した画像を得るためには高度な技術力が必要となるため、通常の医療では3テスラ以下のMRIが使用される(1テスラは10000ガウス)。本研究では、4.7テスラMRIが使用され、100ミクロン程度の分解能で生体の断層画像を得ることができる。
※5 神経膠症(グリオーシス)
外傷や虚血、感染などの侵襲によって生じるグリア細胞の反応である。グリア細胞の肥大や細胞増殖、グリア線維の増加が見られる。グリア性瘢痕(星状細胞増加)に至ることが多い。
※6 グリア
ニューロンと共に、神経組織の二大構成要素である。グリア細胞はニューロンの数の10倍もあり、神経系の体積の約半分を占めると言われている。ニューロンの発達と生存・代謝の支援や、シナプス伝達などに積極的に関わっている。
※7 アストログリア
グリア細胞の一種で、多くの突起を持つことから、星状膠細胞とも呼ばれる。神経線維の支持細胞としての役割を果たす一方で、脳内に異物を取り込まないようにするためのフィルター(血液脳関門)の構成にも関わっているとされる。
問い合わせ先
国立研究開発法人 放射線医学総合研究所 企画部 広報課
Tel:043-206-3026
Fax:043-206-4062
E-mail:05;nfo@nirs.go.jp
