抗精神病薬副作用「高プロラクチン血症」のリスク解明-副作用を回避しながら統合失調症を治療する指標を開発-
平成22年2月23日
独立行政法人放射線医学総合研究所(理事長:米倉義晴)
分子イメージング研究センター※1
菅野 巖センター長、須原 哲也グループリーダー、
荒川 亮介 博士研究員
日本医科大学(学長:田尻 孝)精神医学教室
大久保 善朗 教授の共同研究
概要
陽電子断層撮像装置(PET)※2と高性能PETプローブ※3を用いて、統合失調症治療に不可欠な抗精神病薬※4の主な副作用であり、無月経、排卵抑制などに関連する高プロラクチン血症※5が、下垂体※6ドーパミンD2受容体※7遮断作用により引き起こされることを、世界で初めて明らかにしました。また、抗精神病薬ごとに高プロラクチン血症のリスクが異なることを調べ、リスクを予測する指標を示しました。これまで確認されていなかった抗精神病薬と高プロラクチン血症の関係を人の脳をイメージングすることで証明した世界で初めての画期的な成果です。薬の副作用を回避しながら統合失調症を治療する上で重要な指標とすることができ、今後、分子イメージングによる適切な服薬量設定や合理的な薬物療法など、臨床現場において役立つものと期待されます。
本研究は、文部科学省分子イメージング研究プログラムPET疾患診断研究拠点(研究総括 独立行政法人放 射線医学総合研究所 分子イメージング研究センター長 菅野 巖)の一環として行われました。独立行政法人放 射線医学総合研究所と日本医科大学との共同研究により得られたものであり、米国の精神医学雑誌『The Journal of Clinical Psychiatry』2010年2月23日のオンライン版に掲載されます。
研究の背景と目的
統合失調症は、10代後半から20代前半にかけて発病することが多い精神疾患で人口の約1%が発症し、幻覚・妄想、刺激に対して感情変化や意欲が減退する症状が現れます。統合失調症の治療は薬物療法が中心であり、さまざまな治療薬(抗精神病薬)の開発が進んでいますが、根本的な発症原因や脳内での薬理作用の理解が十分でなく、副作用のひとつである高プロラクチン血症などを予測回避しながら合理的な治療計画を立てるために、客観的な指標の開発が望まれています。
プロラクチンは脳下垂体で分泌されるホルモンで、異常に分泌されると高プロラクチン血症の症状が現れます。症状には、乳汁分泌、無月経、排卵抑制などがあり、長期的には骨粗鬆症や乳がんのリスク増加があります。このホルモンは、下垂体のドーパミンD2受容体で制御されていることが知られています。抗精神病薬がドーパミンD2受容体を遮断することで、分泌が異常に活発になり、高プロラクチン血症が発症すると考えられます。しかしながら、プロラクチン分泌の制御部位である下垂体ドーパミンD2受容体の密度は微少で定量評価が困難であり、これまで十分に研究が行われてきませんでした。
臨床の現場では、抗精神病薬の種類によって高プロラクチン血症のリスクが異なることが経験的に知られています。血管と脳の間には、物質が脳内へ通過する度合いを決める血液脳関門※8があります。下垂体は血液脳関門の外側に位置しているため、血液脳関門を通過して脳内に入りやすい薬剤と入りにくい薬剤では、下垂体に与える影響の度合いが異なります。結果として、副作用である高プロラクチン血症リスクの違いにつながると推測できます。しかし、そのメカニズムを報告した例はこれまでにありません。
研究チームは、高プロラクチン血症のリスクを客観的に評価し、副作用を避けた治療法を実現するため、PETを利用しました。独立行政法人放射線医学総合研究所(放医研)分子イメージング研究センターは、文部科学省の社会のニーズを踏まえたライフサイエンス研究「分子イメージング研究プログラム」のPET疾患診断研究拠点として、研究開発を行っています。このプログラムにより整備した放射性薬剤の合成・製造能力は世界トップクラスを誇り、種類・量ともに多様な研究ニーズに合わせてPETプローブを提供することができます。また、放医研の放射性薬剤は高比放射能※9(高性能化)を実現しているため、微量の分子を高感度で見つけることができます。このような背景により、脳の神経受容体や神経伝達物質の変化を鋭敏に捉えることができます。
高性能化した[11C]FLB457※10を用いて、抗精神病薬の服用による高プロラクチン血症と下垂体ドーパミンD2受容体占有率※11との関係を調べました。さらに、血液脳関門内にある側頭皮質の占有率と比較して、抗精神病薬の種類による高プロラクチン血症の発症リスクについて検討しました。
研究手法と結果
1)研究方法
単一の抗精神病薬を服用中の男性統合失調症患者24名(リスペリドン※127名、オランザピン※137名、ハロペリドール※144名、スルピリド※156名)を対象に[11C]FLB457を用いたPET検査を行い、下垂体および側頭皮質ドーパミンD2受容体占有率を測定しました。また、PET検査直前の血中プロラクチン濃度を測定し、下垂体および側頭皮質ドーパミンD2受容体占有率との関連を検討しました。さらに、下垂体と側頭皮質の占有率から血液脳関門内外の抗精神病薬の濃度比を推定しました。
2)結果
血中プロラクチン濃度と下垂体ドーパミンD2受容体占有率には有意な正の相関が認められましたが(図1)、側頭皮質ドーパミンD2受容体占有率とは相関が認められませんでした。下垂体と側頭皮質のドーパミンD2受容体占有率には、薬剤による傾向の違いが見られました。そこから推定された脳内外の薬物濃度比は、オランザピン(2.7)、ハロペリドール(2.4)、リスペリドン(1.6)、スルピリド(0.3)の順でした(図2)。
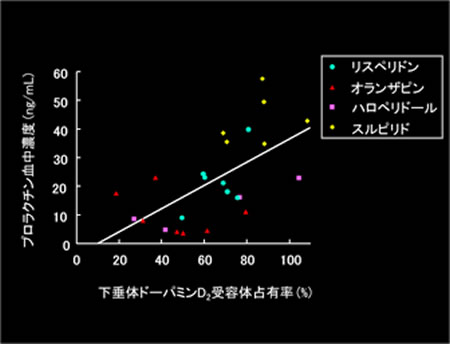
図1 下垂体ドーパミンD2受容体占有率とプロラクチン血中濃度
(Arakawaら,J Clin Psychiatry,2010より改変)
下垂体でのドーパミンD2受容体占有率が高いほど血中プロラクチン濃度も高くなる傾向が示された。
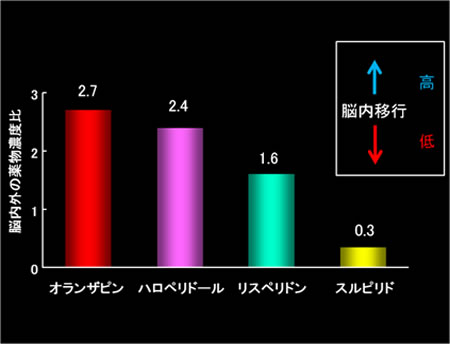
図2 抗精神病薬の脳内外の濃度比(Arakawaら,J Clin Psychiatry,2010より改変)
血液中の薬物濃度を1として、脳内の薬物濃度を示す。この数字が大きいほど血液脳関門を通過して脳内に薬物が入ることを示す。つまり、脳内移行率が高く、高プロラクチン血症のような副作用を起こしにくいことになる。
本研究の成果と今後の展開
本研究では、[11C]FLB457を用いることで下垂体ドーパミンD2受容体占有率を測定することに成功し、血中プロラクチン濃度との正の相関を捉えることができました。抗精神病薬の下垂体ドーパミンD2受容体遮断作用が高プロラクチン血症を引き起こすことを人間の脳で確認した、世界で初めての報告です。これまで臨床的な知識でしかなかった抗精神病薬の副作用である高プロラクチン血症とドーパミンD2受容体遮断作用との関連が、客観的なデータとして提示された世界で初めての画期的なものです。
また、薬剤ごとの血液脳関門を通過しやすいかどうか(脳移行性)の違いが、高プロラクチン血症のリスクと関係していることを示しました。脳内外薬物濃度比が低い薬剤(例えばスルピリド)は、脳内に入りにくく、必要以上に下垂体のドーパミンD2受容体に影響を与え、高プロラクチン血症のリスクが高いと言えます。逆に、脳内外薬物濃度比が高い薬剤(例えばオランザピンやハロペリドール)は、下垂体への影響は少なく、高プロラクチン血症のリスクも比較的低いと考えられます。この傾向は、これまで臨床的に知られていた高プロラクチン血症のリスクとよく一致します(図3)。本研究成果より、下垂体ドーパミンD2受容体占有率が概ね50%以上になると高率で高プロラクチン血症になると考えることができます。
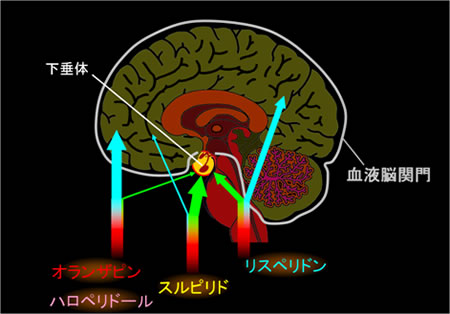
図3 抗精神病薬の脳内移行性
オランザピンやハロペリドールは脳内移行性が高いため、下垂体に与える影響は小さい。一方、スルピリドのように脳内移行性が低い薬剤の場合、下垂体に与える影響も大きくなり、高プロラクチン血症のリスクも大きくなる。
以上のように、PETを用いて下垂体ドーパミンD2受容体占有率を測定することで、高プロラクチン血症を客観的に予測することが可能となりました。今回の成果は、統合失調症の治療に不可欠である抗精神病薬の副作用を回避し合理的な薬物選択や用量設定をする上での重要な指標を開発したといえます。今後は、臨床症例を増やし、明確な副作用閾値を求めるなどして、臨床応用可能な手法として確立していくことが期待されます。
用語解説
※1)分子イメージング
生体内で起こるさまざまな生命現象を外部から分子レベルで捉えて画像化することであり、生命の統合的理解を深める新しいライフサイエンス研究分野。体の中の現象を、分子レベルで、しかも対象が生きたままの状態で調べることができる。がん細胞のふるまいや、アルツハイマー病や統合失調症、うつ病といった脳の病気、「こころの病」を解明し、治療法を確立するための手段として期待されている。
※2)陽電子断層撮像法(positron emission tomography:PET)
レントゲン、CTやMRIと同じ画像診断法の一種で、がんの診断などに用いられる。陽電子を放出する核種で標識した薬剤を注射し、体内から出てくる信号を体の外で捉え、コンピュータ処理によって画像化する技術。
※3)PETプローブ
陽電子断層撮像(PET)装置を用いての、腫瘍や精神・神経疾患の診断・検査等で用いる放射性薬剤。測定したい機能の種類に応じて適切な放射性薬剤を選択する。
※4)抗精神病薬
統合失調症の治療薬。麻酔薬や鎮静剤開発の副産物として偶然見いだされた物質。ドーパミンの受け手となるドーパミンD2受容体が抗精神病薬によって遮断されることで、ドーパミンの神経伝達が阻害され、妄想や幻覚といった症状が治療される。一方、抗精神病薬の服薬量が多くなりドーパミンD2受容体を遮断しすぎると、副作用を生じる。このことから、現在では、ドーパミンD2受容体を遮断しすぎないような類の抗精神病薬が開発されるようになり、それまでの従来型抗精神病薬(第一世代抗精神病薬)と区別して、第二世代抗精神病薬と呼ばれている。
※5)高プロラクチン血症
プロラクチンは下垂体で分泌されるホルモンで、妊娠、授乳、性行動に影響を与える。高プロラクチン血症は、下垂体の腫瘍や薬剤の副作用で認められる。症状として、乳汁分泌、無月経、排卵抑制、性欲低下などがあり、長期的には、骨粗鬆症や乳がんのリスク増加がある。
※6)下垂体
視床下部に接して脳の直下に存在する内分泌器官。プロラクチンの他にも、副腎皮質刺激ホルモン、甲状腺刺激ホルモン、成長ホルモン、性腺刺激ホルモン等の多くのホルモンを分泌する。
※7)ドーパミンD2受容体
ドーパミンは中枢神経系に存在する神経伝達物質で、運動調節・認知機能・ホルモン調節・感情・意欲・学習などに関わると言われている。脳内の線条体と呼ばれる部位において多く認められている。ドーパミンD2受容体は、そのドーパミンと結合する神経受容体、ドーパミン受容体の一つ。
※8)血液脳関門(blood-brain barrier:BBB)
脳血液関門ともいう。血行と脳の間に存在し,特定の物質だけを選択的に通過させる機能的な障壁。毛細血管内皮またはグリア性の膜が関門を構成すると考えられ、ブドウ糖・アルコール・酸素は血液脳関門を通過しやすく、また脂溶性物質や小さい分子は通過しやすい傾向があるが、その機構は未解明の点が多い。
※9)比放射能
ある標識化合物の一定量(μmolまたはμg等)当たりどれだけの放射能(CiまたはGBq等)が含まれているかを示す指標。PETなど分子イメージングの手法で使われる放射性薬剤では、比放射能が高いほど検出精度が向上し、強い生理活性を有する薬剤の標識や生体にごく微量しか存在しない分子のイメージングが可能となる。放医研では世界水準の10~100倍高い比放射能を既に達成している。
※10)[11C]FLB457
高親和性リガンドFLB457のC-11標識体で、ドーパミンD2受容体に結合するリガンド。従来のドーパミンD2受容体用PETプローブでは測定できなかった線条体以外の領域のドーパミンD2受容体の測定に適用可能という特長がある。リガンドとは特定の受容体に特異的に結合する物質のこと。
※11)受容体占有率
脳内の神経伝達を行う部位の一つである受容体への薬物の結合の程度を表す。薬物が受容体に全くないときは0%、すべての受容体に薬物が結合していると100%になる。
※12)リスペリドン
第二世代抗精神病薬であり、統合失調症治療の第一選択薬として用いられる。
※13)オランザピン
第二世代抗精神病薬であり、リスペリドンと同様に第一選択薬の一つ。
※14)ハロペリドール
従来型抗精神病薬の薬剤であり、第二世代抗精神病薬の発売前は最も頻用されていた薬剤の一つ。
※15)スルピリド
従来型抗精神病薬の一つであるが、プロラクチン上昇をきたしやすいとされている。
プレスリリースのお問い合わせ
ご意見やご質問は下記の連絡先までお問い合わせください。
国立研究開発法人 放射線医学総合研究所 企画部 広報課
Tel:043-206-3026
Fax:043-206-4062
E-mail:info@nirs.go.jp
