陽電子断層撮像装置による強迫性障害の病態解明研究
強迫性障害患者の脳内ではセロトニンを
神経細胞内に取り込むタンパク質が減少する
平成21年12月25日
独立行政法人 放射線医学総合研究所
独立行政法人 放射線医学総合研究所(理事長:米倉 義晴)
分子イメージング研究センター※1
菅野 巖センター長、須原 哲也グループリーダー
松本 良平客員協力研究員
成果の概要
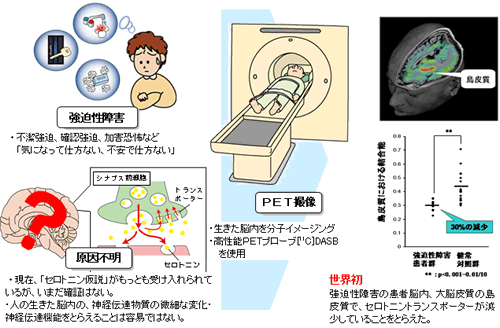
陽電子断層撮像装置(PET※2)と高性能PETプローブ※3を用いて、世界で初めて、強迫性障害※4患者の脳内の大脳外側部位(島皮質※5)で、神経細胞から放出されたセロトニンを細胞内に取り込むタンパク質(セロトニントランスポーター※6)が減少していることを明らかにしました。この成果により、脳内のセロトニンが強迫性障害の原因と病態に関係するとされるセロトニン仮説を支持する証拠が得られました。これに基づいて強迫性障害の脳内メカニズムや病態解析を進め、より詳細な症状や治療法などを検討することで、強迫性障害の原因解明や治療法の開発に貢献できるものと期待しています。
本研究は、文部科学省「社会のニーズを踏まえたライフサイエンス分野の研究開発-分子イメージング研究プログラム-」(PET疾患診断研究拠点、研究総括独立行政法人放射線医学総合研究所菅野巖分子イメージング研究センター長)の一環で実施され、放射線医学総合研究所および東京慈恵会医科大学他との共同研究により成果が得られたものです。米国の脳・神経科学の専門雑誌『NeuroImage』(2010年1月1日号)に掲載されます。
成果のまとめ
「気になって仕方ない・不安で仕方ない」症状(表1)を引き起こす強迫性障害は、生活への影響が極めて高い疾患ですが、原因については解明されていませんでした。
高性能のPETプローブを製造することで、強迫性障害患者の脳内の大脳外側部位(島皮質)で、神経細胞から放出されたセロトニンを細胞内に取り込むタンパク質(セロトニントランスポーター)が減少していることを世界で初めて明らかにしました。
表1:強迫症状の具体例
- 不潔強迫:汚れが気になり、手洗いや入浴の時間や回数が増加する。
一方で、入浴・着替え・掃除を避けるようになり不衛生になる場合も多い。
確認強迫:ドアや窓の鍵、ガスの元栓、水道の蛇口等を閉めたかどうかが、気になってしまい、何回も長時間にわたって、確認してしまう。 - 加害恐怖:自分や他人に危害を加えてしまうかもかもしれないという恐れが強く、何度も打ち消そうと考え込んだり、確認したりする。
- 不完全強迫:左右の対称性や順序の正確性にとらわれて、物事がなかなかはかどらない。
- ため込み強迫:他人からみたらどうでもよい物が、後で必要になるなどと思ってしまい、どうしても捨てられず、物が溜まっていく。
研究の背景と目的
強迫性障害の現状
強迫性障害は、人口の約1-2%が罹患するとされており、強迫観念および強迫行為によって生活が障害される精神疾患です。強迫症状は、「気になって仕方ない・不安で仕方ない」症状です。その症状は多様であり、本人も他人に理解されないという思いから、相談できないケースも多くあります。
強迫性障害は、その90%が15-25歳で発症し慢性に経過することから、生活への影響も極めて高い疾患です。病院を受診し、診断されるまでに発症してから10年以上も経過しているケースも多く、早期発見・治療のために啓蒙が必要な疾患のひとつです。原因については不明な点が多く、いまだに解明されておりません。有望とされているセロトニン仮説※7は、選択的セロトニン再取り込み阻害剤(selective serotonin reuptake inhibitor:SSRI※8)が強迫症状を改善することに基づいていますが、なぜセロトニンを取り込むことを阻害することが有効なのかは不明です。神経細胞から放出されたセロトニンを神経細胞内に取り込むタンパク質がセロトニントランスポーターであり、このタンパク質が脳内のセロトニンの調節を行っています。このことから、強迫性障害患者ではセロトニントランスポーターの変化が起きていることが想定されます。
PETやSPECT※9を用いることで、脳内のセロトニントランスポーター量を計測できます。血流や糖代謝といった脳活動を調べた以前の研究で、強迫性障害では、喜怒哀楽や不安・恐怖といった情動に関連する大脳皮質※10領域の活動の変化が強迫性障害に関与していることが示されました。しかし、以前の研究手法ではセロトニントランスポーターの様な神経伝達機能の微細な変化をとらえることは難しく、また、PETを用いた研究においてもPETプローブの性能が十分でなかったために、大脳皮質のセロトニントランスポーターを調べることはできませんでした。そのため、これまで強迫性障害において、大脳皮質におけるセロトニントランスポーターを調べた研究はありませんでした。
PET疾患診断研究拠点としての放射線医学総合研究所
放射線医学総合研究所(以下、放医研)分子イメージング研究センターは、文部科学省の「社会のニーズを踏まえたライフサイエンス研究-分子イメージング研究プログラム-」のPET疾患診断研究拠点として、平成17年度より分子イメージングの基盤技術の研究開発を行っています。国内随一のPET疾患診断研究拠点として整備した放射性薬剤※11の合成・製造能力は世界トップクラスを誇り、種類・量ともに多様なPETプローブを一日に複数回、人体に投与しても安全な品質を維持し提供できる設備と技術を有しています。また、放医研の放射性薬剤は、比放射能※12が高く、脳の神経受容体や神経伝達物質の変化を他の施設よりも鋭敏に捉えることが可能です。
このような放医研の成果や基盤技術を背景に、松本らの研究チームは、PET装置と高性能PETプローブを用いて、大脳皮質におけるセロトニントランスポーターを測定しました。近年開発された[11C]DASB※13というPETプローブは、従来のPETプローブよりも性能が高く、これまで不可能だった大脳皮質においてセロトニントランスポーターを測定することができます。この[11CC]DASB特有の長所に加えて、放医研で開発したデータ解析方法を用いることで、世界で初めて強迫性障害において大脳皮質でのセロトニントランスポーターの減少を捉えることに成功しました。
研究手法と結果
本研究では10名の強迫性障害患者と18名の健常対照者に[11C]DASBを用いたPET検査により脳内のセロトニントランスポーターの量(結合能※14)を測定し、脳内の様々な部位での結合能を比較検討しました。その結果、強迫性障害患者群では、健常対照群と比較して、大脳皮質の島皮質でセロトニントランスポーターの減少が認められました(図1-2)。
![MRIと[11C]DASBを用いたPET画像の重ね合わせによる大脳 皮質の島皮質領域の図示。](/uploaded/image/2542.jpg)
図1 MRIと[11C]DASBを用いたPET画像の重ね合わせによる大脳皮質の島皮質領域の図示。
![強迫性障害患者群では、大脳皮質の島皮質での[11C]DASB 結合能 (セロトニントランスポーターの量) の平均値が、健常対照群に比べて、30%減少していることが分かり ました。](/uploaded/image/2543.png)
図2 強迫性障害患者群では、大脳皮質の島皮質での[11C]DASB結合能(セロトニントランスポーターの量)の平均値が、健常対照群に比べて、30%減少していることが分かりました。
本研究成果と今後の展望
強迫性障害群では健常対照群に較べて島皮質のセロトニントランスポーターが減少していました。島皮質は、大脳の外側面の奥に、前頭葉・側頭葉・頭頂葉の一部によって覆われている領域です。島皮質は、近年、不安・不快感・恐怖といった情動に重要な役割を果たすと考えられるようになってきています。これらのことを合わせると、島皮質でのセロトニン神経機能が強迫性障害の病態、特に不安症状に重要な役割を担っていると考えられます。
今回の成果は、強迫性障害のセロトニン仮説を支持するものであると同時に大脳皮質におけるセロトニンが強迫性障害に関与していることを示唆する点で画期的であると考えられます。強迫性障害を含めた精神疾患では、原因が不明なものが多く、また、客観的な指標に乏しいことが現実です。今回の研究のようにPETを用いることで精神疾患の原因解明や治療法の開発に大きく貢献することが期待されます。
用語解説
※1)分子イメージング
生体内で起こるさまざまな生命現象を外部から分子レベルで捉えて画像化することであり、生命の統合的理解を深める新しいライフサイエンス研究分野。体の中の現象を、分子レベルで、しかも対象が生きたままの状態で調べることができる。がん細胞のふるまいや、アルツハイマー病や統合失調症、うつ病といった脳の病気、「こころの病」を解明し、治療法を確立するための手段として期待されている。放射線医学総合研究所分子イメージング研究センターは、文部科学省委託事業分子イメージング研究プログラムのPET疾患診断研究拠点として研究活動を行っている。
※2)陽電子断層撮像法(positron emission tomography:PET)
レントゲン、CTやMRIと同じ画像診断法の一種で、がんの診断などに用いられる。陽電子を放出する核種で標識した薬剤を注射し、体内から出てくる信号を体の外で捉え、コンピュータ処理によって画像化する技術。
※3)PETプローブ
放射性薬剤※11のうち、陽電子断層撮像(PET)装置を用いて腫瘍や精神・神経疾患の診断・検査等で用いられるもの。測定したい機能の種類に応じて適切なPETプローブを選択するが、本研究では[11C]DASB※13を用いている。
※4)強迫性障害
強迫性障害は、人口の約1-2%が罹患するとされており、強迫観念および強迫行為によって生活が障害される精神疾患。10-20歳代に発症することが殆どであるが、その症状は多様であり(本文中表1参照)、相談することが出来ずに長期に経過している例も多い。症状が重症化すると、日常生活にも支障を来たす様になり、長期の引きこもりを呈する場合もある。SSRI※8を主剤とした薬物療法と認知行動療法による治療が有効である。
※5)島皮質
大脳の外側面の奥に、前頭葉・側頭葉・頭頂葉の一部によって覆われている領域で、近年、不安・不快感・恐怖といった情動に重要な役割を果たすと考えられるようになってきている。
※6)セロトニントランスポーター
神経細胞から放出されたセロトニンを細胞内に取り込むタンパク質。細胞外のセロトニン濃度の低下がうつ病の原因の1つとされており、フルボキサミンのようにセロトニントランスポーターに結合しセロトニンの再取り込みを阻害する薬剤は抗うつ効果を発揮すると考えられている。
※7)セロトニン仮説
選択的セロトニン再取り込み阻害薬(selective serotonin reuptake inhibitor:SSRI※8)が、うつ病のみならず強迫性障害の治療にも有用なことから、脳内のセロトニンが強迫性障害の原因および病態に関係しているという仮説。
※8)選択的セロトニン再取り込み阻害薬(selective serotonin reuptake inhibitor:SSRI)
セロトニンは中枢神経系に存在する神経伝達物質で、睡眠調節、体温調節、気分、食欲、性欲などに関わると言われている。選択的セロトニン再取り込み阻害薬は、セロトニントランスポーターという、神経細胞から放出されたセロトニンを細胞内に取り込むタンパク質に選択的に結合し、セロトニンの細胞内への再取り込みを阻害する抗うつ薬。
※9)SPECT
単一光子放射断層撮影(Single photon emission computed tomography:SPECT)人体の画像診断法の一つで、通常は略してスペクト(SPECT)と呼ぶ。体内に投与した放射性同位体から放出されるガンマ線を検出し、その分布を断層画像にしたもの。PET※2と同じく、生体のさまざまな機能を観察することを目的に使われ、従来のCT装置では確認できなかった血流量や代謝機能の情報が得られるため、脳血管障害、心臓病、癌の早期発見に有効とされる。
※10)大脳皮質
大脳の表面に広がる神経細胞の灰白質の層である。大脳基底核と呼ばれる白質の周りを覆っている。知覚、随意運動、思考、推理、記憶など、脳の高次機能を司る。
※11)放射性薬剤
放射性薬剤とは、放射性同位元素で標識された化合物のこと。分子の一部分を、F-18(フッ素18)やC-11(炭素11)など、放射線を放出する核種(放射性同位元素、ラジオアイソトープ)で標識し、代謝や化学反応による放射性薬剤の体内分布の変化を放射線の検出によりとらえる。
※12)比放射能
比放射能とは、ある標識化合物の一定量(μmolまたはμg等)当たりどれだけの放射能(CiまたはGBq等)が含まれているかを示す指標。PETなど分子イメージングの手法で使われる放射性薬剤では、比放射能が高いほど検出精度が向上し、強い生理活性を有する薬剤の標識や生体にごく微量しか存在しない分子のイメージングが可能となる。放医研では世界水準の10-100倍高い比放射能を既に達成している。
※13)[11C]DASB
セロトニントランスポーターに選択的に結合する化合物であるDASBをC-11という放射性同位元素で標識したもの。PETプローブ※3としてセロトニントランスポーターの定量に用いられている。
※14)結合能
受容体の数と親和性を表す総合的な指標(binding potential:BP)。
プレスリリースのお問い合わせ
ご意見やご質問は下記の連絡先までお問い合わせください。
国立研究開発法人 放射線医学総合研究所 企画部 広報課
Tel:043-206-3026
Fax:043-206-4062
E-mail:info@nirs.go.jp
