平成27年11月5日
国立研究開発法人放射線医学総合研究所(理事長:米倉 義晴)
分子イメージング研究センター先端生体計測研究プログラム
山谷 泰賀チームリーダー
本研究成果のポイント
- 独自の半球状検出器配置で検出器数1/5でも3倍感度を達成
- 微量な認知症の原因タンパク質の画像化による早期診断に期待
国立研究開発法人 放射線医学総合研究所(理事長:米倉義晴、以下、放医研)と、株式会社アトックス(代表取締役社長:矢口敏和)の研究チームは、世界初となるヘルメット型PETの開発に成功しました。

超高齢化社会を目前にした認知症対策として、PET※1による早期診断等の実現が期待される一方、脳内のごく微量な原因タンパク質を検出する上で、従来のPET装置の感度や解像度は十分とは言えません。感度を上げるには検出器を測定対象に近づける必要がありますが、従来の検出器はそれにより解像度が劣化してしまいます。そこで近づけても解像度を維持できる独自技術である3次元放射線検出器(DOI検出器)※2を、頭部に最も近づくよう、世界で初めてヘルメット型(半球状)に配置した頭部専用PET装置を開発しました(特開2015-087260)。従来の円筒型の全身用PET装置と比較した場合、近接化により3倍以上感度が向上し、微量な脳内タンパク質の画像化も可能になります。検出器数も1/5に削減でき、従来技術では相容れることがない高性能化と低価格化を同時に実現できる可能性があります。高性能、小型かつ低価格で導入、設置がしやすいヘルメット型PETは、認知症早期診断の普及に役立つと期待されます。本成果の詳細は、第55回日本核医学会学術総会(東京、11月5日~7日)で報告されます。
背景と目標
日本を始め高齢化が進む先進国において、アルツハイマー病をはじめとする認知症対策は喫緊の課題です。認知症等を早期に発見することにより、病気の進行度合いを本人や周囲が把握して、症状の進行抑制や介護等適切な対応が可能となります。そのため、PETによる認知症早期診断の実現が期待されており、PET装置についても大きな需要が見込まれます。認知症の早期では微量な原因タンパク質をPETで画像化するのに十分な解像度と感度が必要です。しかし、従来の全身用PET装置はそれらが十分でないほか、高価・大型のため普及には限界があります。感度を上げるには検出器を測定対象に近づける必要がありますが、従来の検出器はそれにより解像度が劣化してしまいます。そこで本研究チームは、放医研の独自技術である、近づけても解像度を維持できる3次元放射線検出器(DOI検出器)の特性を活かして、高解像度・高感度・コンパクト・低価格な頭部専用PET装置の実現を目標としました。
原理
高感度の実現には、検出器を測定対象に近づける必要がありますが、従来検出器は近づけると解像度が劣化してしまうため、これまでのPETはすべて大口径の円筒型検出器配置でした(図1(a))。そこで本研究では、近づけても解像度を維持できるDOI検出器を用いて、頭部に最も検出器を近づけるようにしました(図1(b))。具体的には、半球状に検出器を並べたヘルメット部(内径25cm、外径50cm)のほかに、あご部にも帽子のあごひものように検出器を追加配置することで、脳の中心部の感度も高めています(特開2015-087260)。
また、検出器の使用数(54個)は、一般的な従来装置に比べて約1/5と少ないため、装置価格を下げることができ、低コストの実現が可能となります。
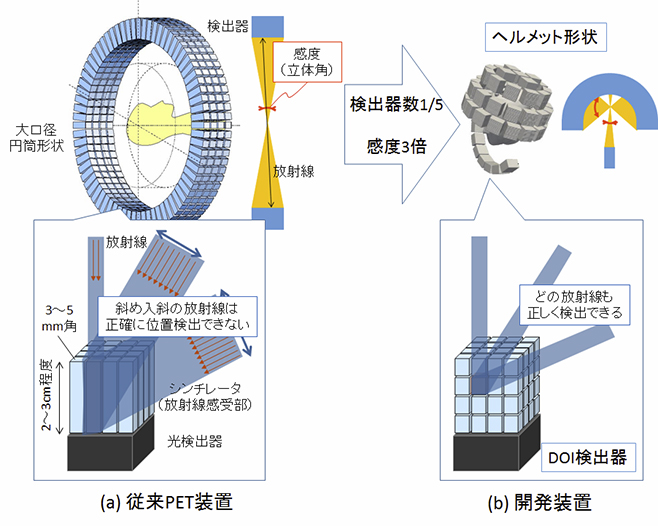
図1 従来装置(a)と開発装置(b)の原理の比較
従来装置は、シンチレータ※3の厚みにより斜め入射の放射線が発せられた位置を正確に検出できません。これによる画質の低下を回避するため、放射線がなるべく垂直に入射するよう、大口径の円筒状に検出器を配置しています。そのため立体角は小さく、感度(ある地点から放出された放射線が検出器に入射する確率)は低くなり、検出器も多数必要となります。
一方、DOI検出器は入射方向によらず正確に放射線が発せられた位置を検出できます。したがって、頭部に検出器を最も近接させて立体角を大きくしたヘルメット形状の配置が可能となり、3倍以上の感度を従来装置の約1/5の検出器数で得られました。
開発成果と今後の展望
開発装置の外観と内部の検出器配置をそれぞれ図2(a)と(b)に示します。性能試験の結果、装置感度は脳中央部でも5%、脳表部では10%(従来装置の約3倍)と高く、場所によらず均一な3mm以下の解像度が達成できました(図2(c))。
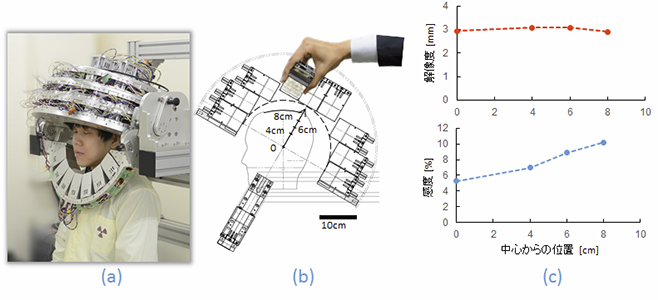
図2 開発装置の外観(a)と内部の検出器配置(b)最大10%以上(従来装置の約3倍)の装置感度と、3mm以下の解像度が得られました(c)。
糖代謝を調べる市販のPET検査薬であるFDG※4を用いた健常ボランティア試験の画像を図3に示します。
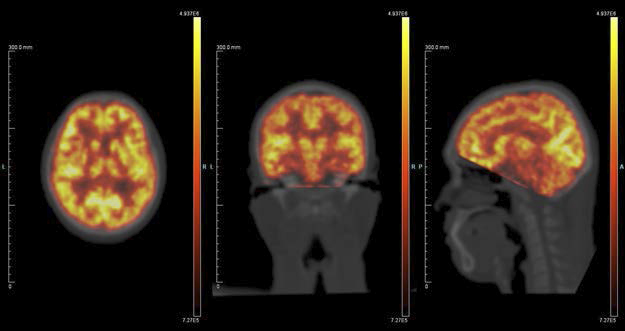
図3 糖代謝を調べる市販のPET検査薬であるFDGを用いた健常ボランティア試験の結果(3つの断面を表示)別途取得したCT画像の上にPET画像を重ねて表示しています。
感度が高いほど多くの放射線を検出器でき、良い画質が得られます。これにより、認知症の発症前から早期では、蓄積量がわずかであると考えられている脳内の原因タンパク質の量や分布を画像化できると期待される他、感度が高い分だけ、検査時間の短縮やPET薬剤の少量化による被ばくの低減も可能になります。
また、ヘルメット型の検出器配列により、検出器数を減らすことができるので装置の低価格化を実現できる可能性があります。それに加えて、検査時の姿勢を座位にしたことにより、一般的な従来PET装置と比べて、開発装置は非常にコンパクトで設置場所に余裕がない病院でも導入しやすいサイズになりました(図4)。
PET薬剤の少量化や検査時間の短縮は患者にとって有益であるだけでなく、病院や検査機関においては数多く検査を実施できるという利点があります。これらを可能にする高性能、小型で低価格化も見込めるヘルメット型PETは、認知症PET診断の普及に役立つと期待できます。今後も研究開発を継続し、検出器の改良によって1mmに迫る高い解像度を目指すことでこれまでのPET検査では見えなかった、脳深部にある記憶の座である海馬と呼ばれる領域での加齢によるアルツハイマー病の原因とされる異常なタンパク質の蓄積のプロセスや、大脳皮質の層構造や脳幹部などの様々な神経細胞の分布などが見えるようになると考えられ、神経変性疾患や精神神経疾患の病態、脳の機能を明らかにできると期待されます。
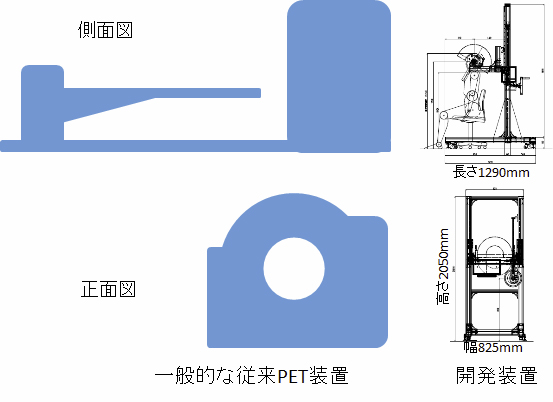
図4 一般的な従来PET装置(左)と開発装置(右)の大きさの比較
用語解説
※1 PET
陽電子断層撮影法(Positron Emission Tomography)の略称。身体の中の生体分子の動きをそのままの状態で外から見ることができる画像診断法の一種。特定の放射性同位元素で標識したPET薬剤を検査対象者に投与し、PET薬剤より放射される陽電子に起因するガンマ線を検出することによって、体深部に存在する生体内物質の分布や量、時間変化を測定できる。
※2 3次元放射線検出器(DOI検出器)
次世代のPETの技術開発において、放医研が世界に先駆けて開発した新規検出器であり、従来の2次元の放射線位置検出に対して、検出素子の深さ方向も含めて3次元の放射線位置検出を可能とする。従来のPETでは両立できなかった感度と解像度の双方を飛躍的に向上させることができる。
※3 シンチレータ
放射線が当たると蛍光(シンチレーション光)を出す物質のこと。
※4 FDG
ブドウ糖に類似したフルオロデオキシグルコース(FDG)を放射性同位元素のフッ素-18(18F)で標識したPET薬剤。がん診断・検診のために広く用いられている。
