量子科学技術で作る未来 第41回
中皮腫 治療薬候補を開発
量子科学技術研究開発機構(QST)は、中皮腫に対するアルファ(以下、α)線放出核種を用いた核医学治療薬候補の開発に成功し、動物実験でその抗がん効果を明らかにした。
中皮腫は、胸膜などにある中皮から発生する悪性腫瘍で、80-85%が胸膜から発生する。中皮腫の原因のほとんどは、アスベストばく露である。2005年のクボタショックを契機に大きな社会問題となった。日本国内における中皮腫による死亡者数は増加の一途をたどっており、アスベストばく露から発症までの潜伏期間が25~50年とされている。悪性中皮腫の発生ピークは2030年頃、罹患者数は年間3,000人に及ぶと予測されている。診断される患者の7割以上が進行がんであり、有効な治療法がなく予後が悪いため、新たな治療法が望まれている。
我々は、放射線の飛ぶ距離が細胞数個分で、当たった細胞を殺傷する能力が高いα線を放出する核種アクチニウム225(以下、225Ac)を加速器で効率よく製造することに成功している。225Acは、近年、前立腺がんの画期的な治療薬として注目されている核医学治療用の放射線同位体である。
この225Acを中皮腫細胞だけに届けることができれば、周囲の正常細胞を傷つけることなく、がん細胞を殺傷することが可能である。そこで、我々は、中皮腫細胞の細胞表面に多く存在しているポドプラニンというタンパク質に結合する抗体NZ-16(以下、「NZ-16」という。)に、225Acを結合したα線核医学治療薬候補として225Ac結合NZ-16を開発した。ポドプラニンは中皮腫の中でも悪性度が高い肉腫型にも高発現しているタンパク質で治療標的として有望である。
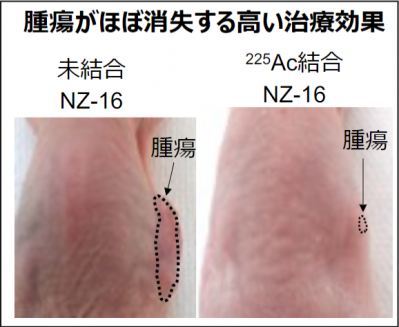
225Ac結合NZ-16を、中皮腫のモデルマウスに1回投与したところ、腫瘍サイズを縮小させ、ほぼ消失する効果があることを確認した。また、生存期間を延長することも確認した。一方で、副作用の指標となる体重減少や病理所見は認められなかった。これらの研究成果から、悪性中皮腫に対して、225Ac結合NZ-16によるα線核医学治療が副作用の少ない効果的な治療法となることが期待される。現在、臨床応用に向けて関係機関と協力して準備を進めており、3年後の臨床試験の実施を目指している。
執筆者
量子科学技術研究開発機構 量子生命・医学部門 量子医科学研究所 分子イメージング診断治療研究部
核医学基礎研究グループ グループリーダー

辻 厚至(つじ・あつし)
非密封放射性同位元素を利用した核医学の診断・治療の開発研究に従事している。がん治療法のひとつ、抗体を利用した放射免疫治療法の開発研究に注力している。
本記事は、日刊工業新聞 2022年4月14日号に掲載されました。
■日刊工業新聞 量子科学技術でつくる未来(41)中皮腫 治療薬候補を開発(2022年4月14日 科学技術・大学)
