グループリーダー
小西 輝昭

メンバー
・上原章寛 主幹研究員
・田中泉 主任研究員
・薬丸晴子 研究員
・城鮎美 主任研究員(併任)
・間宮大晴 スチューデントリサーチャー(SR)(立教大学・連携大学院生D2)
・業務補助員 3名
・専門業務員 1名 (併任)
研究内容
内部被ばく後の除染法や治療技術の高度化研究
私たちはウランなどの放射性核種による内部被ばくの低減化を目指して研究を行っています。
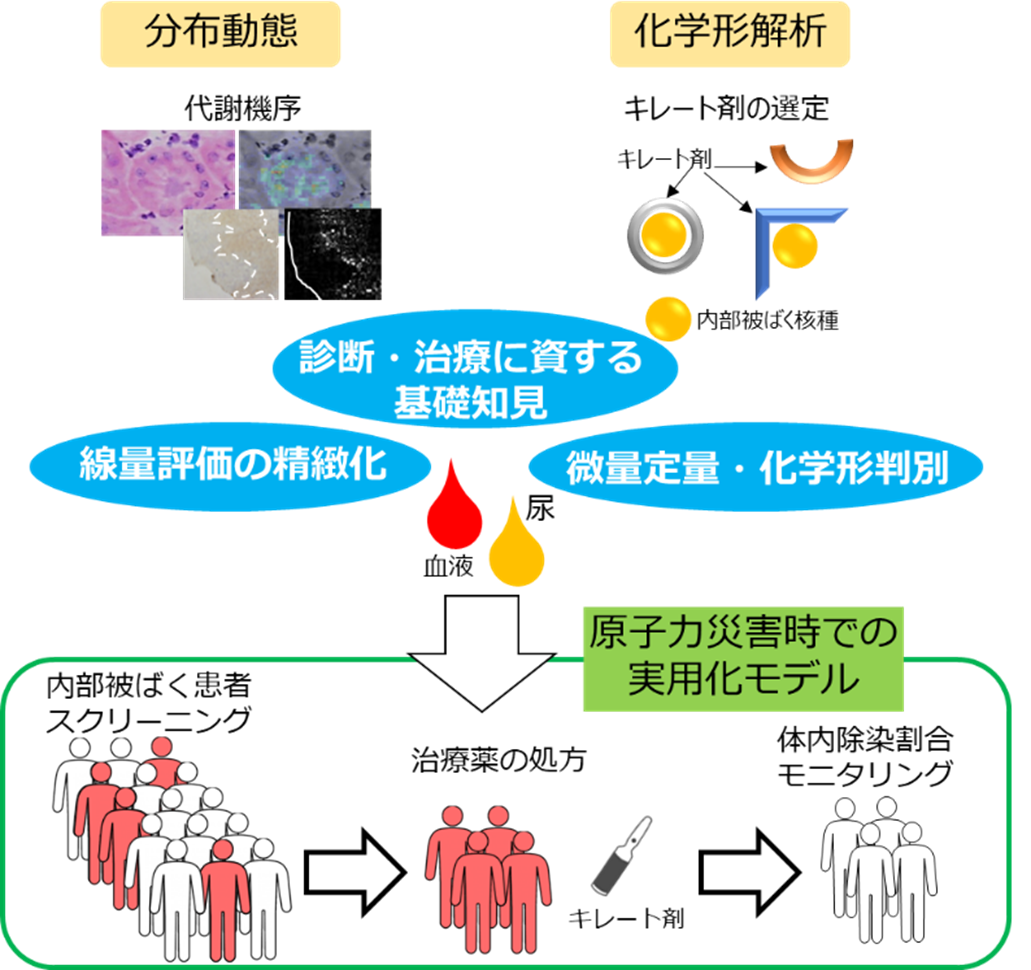
本グループでは、大型放射光施設SPring-8や静電加速器などの先端的な量子ビームを活用したXAFS分析法やマイクロPIXE分析法によって、放射性核種の体内分布、代謝機序および生体内化学形を分子・細胞レベルから個体レベルのスケールで詳細に解析しています。微量元素定量や高精度の被ばく線量の評価が可能になり、適切な治療法の開発につながることが期待されます。
さらに、放射性核種の内部被ばくは、その化学的毒性と放射線障害の両方の作用をもたらすと考えられることから、マイクロビーム細胞照射装置を活用し、様々な放射線種による生物影響についても、細胞レベルでの防御的な細胞応答機構の解明に向けた研究を実施しています。
放射性核種の体外排泄治療薬を用いた除染評価手法を開発し、原子力災害時での内部被ばく患者のスクリーニングおよび体内除染モニタリングに役立てます。この研究成果は、内部被ばくによる体内除染治療に有用な情報を提供します。
放射線医科学研究基盤高度化のための国際共同プロジェクト
世界15機関による国際連携体制で実施されている国際原子力機関国際共同プロジェクト(IAEA-CRP F11024)に参加しています。
プロジェクト目的は、単一細胞の高分解能イメージングと照準照射を可能にするマイクロビーム照射技術による放射線治療・医科学研究基盤の高度化と研究推進です。
当該グループは、所内外・国内外の研究グループと連携して、陽子線とα線の生物効果を単一細胞レベルで解析し、放射線障害低減および緊急被ばく医療の高度化に資する研究を推進しています。静電加速器棟マイクロビーム細胞照射装置SPICEは、IAEA-CRPにおける放射線生物学研究の重要な役割を担っています。
以下は、参加国(機関)リストとQST千葉地区で開催された第二回企画会議の参加者です。
(IAEA-CRP F11024 “Sub-cellular Imaging and Irradiation using Accelerator-based Techniques.” Project Duration 2023 May 19 – 2028 July 1)


↵
List of Papers
- 解説記事:小西輝昭. IAEA国際共同研究プロジェクト:マイクロビーム照射技術の高度化による放射線医科学・がん治療研究への貢献. Isotope News. 2025; 797: 18-21.
- Autsavapromporn N, Mamiya T, Liu C, Duangya A, Tengku Ahmad TA, Oikawa M and Konishi T (2026) Bystander effects in both hypoxic cancer and normal cells under FLASH irradiation using proton microbeams. Int J Radiat Biol. 1-13.DOI: 10.1080/09553002.2026.2654422
- Mamiya T, Kusumoto T, Sasai K, Kamiguchi N, Amano D, Kurita K, Kodaira S and Konishi T (2025) Ultra-high dose rate protons in clinical irradiation suppress DNA single-strand breaks induction in the below nano-second time scale of physicochemical stages. Int J Radiat Biol. 101: 1098-1104. DOI: 10.1080/09553002.2025.2548470
- Kirishima A, Takei M, Uehara A and Akiyama D (2025) Determination of the thermodynamic quantities for complex formation of U(VI) with amino acids in aqueous solution. J. Chem. Thermodyn. 206: 107469.DOI: 10.1016/j.jct.2025.107469
- Yakumaru H, Kato Y, Oikawa M, Numako C, Ohsawa D, Tanaka I, Uehara A, Ishihara H and Homma-Takeda S (2024) Micro-PIXE imaging of the rib bones of rats. Nucl. Instr. Meth. B. 553: 165386.DOI: 10.1016/j.nimb.2024.165386
- Uehara A, Tanaka I, Ishihara H, Akiyama D, Kirishima A and Homma-Takeda S (2024) Monitoring method for uranium concentration and chemical form in the droplet of rat serum. J Toxicol Sci. 49: 543-548.DOI: 10.2131/jts.49.543
- Fujii T, Kato C, Wada N, Uehara A, Sossi P and Moynier F (2023) Theoretical and Experimental Study on Vanadium Isotope Fractionation among Species Relevant to Geochemistry. ACS Earth Space Chem. 7: 912-925.DOI: 10.1021/acsearthspacechem.2c00299
- Konishi T, Wang J, Kobayashi A, Liu C, Hiroyama Y, Mamiya T, Kusumoto T and Oikawa M (2025) Microbeam irradiation reveals cytoplasmic damage contributes to micronuclei induction. The European Physical Journal Plus. 140.
- Wang J, Oikawa M and Konishi T (2023) Stimulation of Nuclear Factor (Erythroid-Derived 2)-like 2 Signaling by Nucleus Targeted Irradiation with Proton Microbeam. Biology (Basel). 12.
- Konishi T, Kusumoto T, Hiroyama Y, Kobayashi A, Mamiya T and Kodaira S (2023) Induction of DNA strand breaks and oxidative base damages in plasmid DNA by ultra-high dose rate proton irradiation. Int J Radiat Biol. 99: 1405-1412.
- Uehara A, Matsumura D, Tsuji T, Yakumaru H, Tanaka I, Shiro A, Saitoh H, Ishihara H and Homma-Takeda S (2022) Uranium chelating ability of decorporation agents in serum evaluated by X-ray absorption spectroscopy. Anal Methods. 14: 2439-2445. DOI: 10.1039/d2ay00565d
- Kobayashi A, Hiroyama Y, Mamiya T, Oikawa M and Konishi T (2023) The COX-2/PGE2 Response Pathway Upregulates Radioresistance in A549 Human Lung Cancer Cells through Radiation-Induced Bystander Signaling. Biology (Basel). 12.
- Autsavapromporn N, Kobayashi A, Liu C, Jaikang C, Tengku Ahmad TA, Oikawa M and Konishi T (2022) Hypoxia and Proton microbeam: Role of Gap Junction Intercellular Communication in Inducing Bystander Responses on Human Lung Cancer Cells and Normal Cells. Radiat Res. 197: 122-130.
- Wang J and Konishi T (2019) Nuclear factor (erythroid-derived 2)-like 2 antioxidative response mitigates cytoplasmic radiation-induced DNA double-strand breaks. Cancer Sci. 110: 686-696. DOI: 10.1111/cas.13916
- Konishi T, Kodaira S, Itakura Y, Ohsawa D and Homma-Takeda S (2019) Imaging Uranium Distribution on Rat Kidney Sections through Detection of Alpha Tracks Using Cr-39 Plastic Nuclear Track Detector. Radiat Prot Dosim. 183: 242-246.
- Konishi T, Oikawa M, Suya N, Ishikawa T, Maeda T, Kobayashi A, Shiomi N, Kodama K, Hamano T, Homma-Takeda S, Isono M, Hieda K, Uchihori Y and Shirakawa Y (2013) SPICE-NIRS microbeam: a focused vertical system for proton irradiation of a single cell for radiobiological research. J Radiat Res. 54: 736-747.DOI: 10.1093/jrr/rrs132
